题目内容
(20003牟南京质检题)20℃、1.0lXl05Pa时,将ALHCI气体溶于BL水中,形成了密度为ρg·cm-3的盐酸。设该条件下气体摩尔体积为ymL·mol-1。用含字母的代数式表示:
(1)盐酸中HCI的物质的量浓度。
(2)取上述所得盐酸体积的十分之一跟足量的锌粒反应,在20℃、1.01×105Pa时可产生多少升氢气?
答案:
解析:
解析:
(1) 求溶液的物质的量浓度,即求出溶质的物质的量,A/22.4mol,溶液的体积为(B×103×1+A/22.4×36.5)÷ρ×10-3L,则得出溶液的物质的量浓度为:
(2)跟锌反应的氯化氢的物质的量为:A/22.4×0.1mol,则产生氢气的体积为:A/22.4×0.1×1/2×22.4L/mol=0.05L
|

练习册系列答案
相关题目
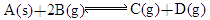 已达平衡的是
已达平衡的是