题目内容
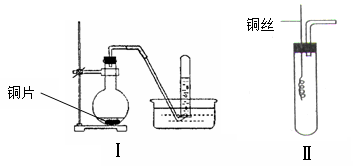
(12分)下图是铜与稀硝酸反应的两个实验装置图,请回答下列问题:
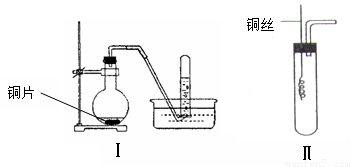
(1)铜与稀硝酸反应的化学方程式_____ _ 。
(2)学生甲用装置Ⅰ探究铜与稀硝酸反应的气体产物。实验过程在烧瓶中观察到有红棕色气体产生,在试管中收集到无色气体。
烧瓶中产生红棕色气体的原因是 (用方程式表示) 。
(3)学生乙认为,甲用装置Ⅰ实验,无法说明问题。为了证明并观察到铜与稀硝酸反应的产物为NO,甲设计了如图Ⅱ所示的实验装置,选择下列药品,并按下列实验步骤完成该实验。请你根据他的思路,回答下列问题:
药品:稀硝酸 锌粒 石灰石固体
步骤:
①检查装置的气密性
②向试管中加入一定量CaCO3固体
③向试管中倒入过量的稀HNO3并迅速盖上带铜丝和导管的橡皮塞
④待反应完全后,将导管插入试管内接近液面
⑤将铜丝插入到溶液中
⑥用注射器的针头穿过橡皮塞并向试管内推入氧气(或空气)
(ⅰ)步骤①②目的是 ;
(ⅱ)推入氧气或空气的目的是 ;
(ⅲ)分别将等质量的铜片与等体积均过量的浓硝酸和稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出,这可能是Cu2+的浓度差异引起的,你同意这种看法吗? (填“同意”或“不同意”),原因是 。
.(1)3Cu + 8HNO3 3Cu(NO3)2
+ 2NO↑+ 4H2O
(2)2NO+ O2 ===== 2NO2
(3)(ⅰ)排除装置中的氧气
(ⅱ)检验生成的NO气体
(ⅲ)不同意,铜片质量相同,该液体体积相同;生成的Cu2+浓度相同。
【解析】(1)稀硝酸具有氧化性,能氧化铜生成硝酸铜,NO和水,反应式为3Cu + 8HNO3=3Cu(NO3)2 + 2NO↑+ 4H2O。
(2)装置中含有空气,能把NO氧化生成NO2,所以会出现红棕色,反应式为2NO+ O2 =2NO2。
(3)要得到NO,就必须防止被氧气氧化,所以要利用反应中产生的CO2来排尽装置中的空气。通过注入氧气或空气可以验证反应中产生的NO气体。由于硝酸都是过量的,而参加反应的铜是相同的,所以生成的硝酸铜也是相同的,即浓度是相等。