题目内容
R为1~18号元素中的一种非金属元素,若其最高价氧化物对应水化物的化学式为HnROm,则此时R元素的化合价为 ,R原子的最外层电子数为 ,其气态氢化物的化学式为 .
考点:原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:在一般的化合物中,O元素显-2价、H元素显+1价,化合物中各元素化合价的代数和为0,据此判断R元素化合价;主族元素中,元素最高正化合价与其最外层电子数相等,其最低负化合价=最外层电子数-8.
解答:
解:在一般的化合物中,O元素显-2价、H元素显+1价,化合物中各元素化合价的代数和为0,所以R元素化合价为+(2m-n);主族元素中,元素最高正化合价与其最外层电子数相等,所以其最外层电子数=2m-n,其最低负化合价=最外层电子数-8=2m-n-8,所以其氢化物的化学式为H8-2m+nR,故答案为:+(2m-n);2m-n;H8-2m+nR.
点评:本题考查了原子结构和元素性质,明确元素最高正化合价与其最外层电子数、族序数、最低负价之间的关系是解本题关键,注意第一个空中要写上“+”,为易错点.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
分类是化学学习与研究的常用方法,下列分类正确的是( )
| A、Na2O、MgO、Al2O3均属于碱性氧化物 |
| B、根据电解质在水溶液中电离的程度,将电解质分为强电解 质和弱电解质 |
| C、根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D、石灰石、生石灰、熟石灰均属于碱 |
有a、b、c 3种金属,将a、b放在稀硫酸中,用导线连接,电流方向由a到b.把a放在c的硫酸盐溶液中,a表面有c析出.这3种金属的活动性顺序是( )
| A、b>a>c |
| B、a>b>c |
| C、c>b>a |
| D、c>a>b |
设N0为阿伏加德罗常数值,下列有关叙述不正确的是( )
| A、常温常压下,1mol甲基(一 CH3)所含的电子数为10N0 |
| B、0.4mol以任意比例混合的乙炔和乙醛混合气体,在氧气中充分燃烧.消耗氧气的分子数为N0 |
| C、常温常压下,N0个甲烷分子的体积大于22.4L |
| D、1mol Na2O2与水反应时,转移的电子数为2N0 |
 .有机物X的键线式为:
.有机物X的键线式为:
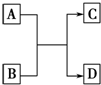 已知A、B、C、D分别是由短周期元素组成的四种微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒.请回答下列问题:
已知A、B、C、D分别是由短周期元素组成的四种微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒.请回答下列问题: