题目内容
【题目】下图是CH4、CCl4、CH3Cl (沸点:-24.2℃)的球棍模型图。下列说法正确的是( )
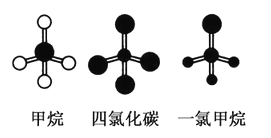
A. CH4、CCl4和CH3C1都是正四面体结构
B. 标准状况下,2.24L一氯甲烷含有的分子数为6.02×1022
C. 甲烷与氯气的取代反应,生成的产物中CH3C1最多
D. 四氯化碳是一种常见的有机溶剂,密度比水小
【答案】B
【解析】A. CH3C1中C-H键与C-Cl键的键长不等,是四面体结构,但不是正四面体结构,故A错误;B. 标准状况下,2.24L一氯甲烷的物质的量为0.1mol,含有的分子数为6.02×1022,故B正确;C. 甲烷与氯气的取代反应,生成的产物与甲烷和氯气的物质的量之比有关,故C错误;D. 四氯化碳的密度比水大,故D错误;故选B。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【题目】草酸钴用途广泛,可用于指示剂和催化剂制备。一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4·2H2O工艺流程如下:
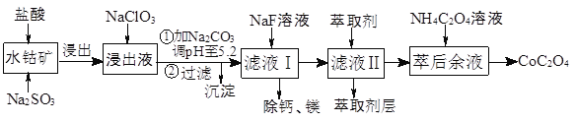
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3的目的是将_____________还原(填离子符号)以便固体溶解。该步反应的离子方程式为 (写一个)。
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,氯元素被还原为最低价。该反应的离子方程式为 。
(3)利用平衡移动原理分析:加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是 。
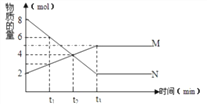
(4)萃取剂对金属离子的萃取率与pH的关系如图所示。滤液Ⅱ中加入萃取剂的作用是 ;使用萃取剂适宜的pH=____(填序号)左右:
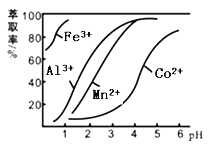
A.2.0 B.3.0 C. 4.0
(5)滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)= 。