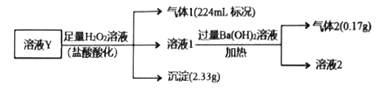
题目内容
【题目】(1)常温下,将1 mL pH=1的H2SO4溶液加水稀释到100 mL,稀释后的溶液中![]() =________。
=________。
(2)某温度时,测得0.01 mol·L-1的NaOH溶液的pH=11,则该温度下水的离子积常数KW=____________,该温度____________25 ℃。(填“>”、“=”或“<”)
(3) 在(2)所述温度下,将pH=12的NaOH溶液Va L与pH=2的硫酸Vb L混合。若所得混合液的pH=10,则Va∶Vb=___________。
(4) 常温下,将1mL pH均为11的氨水与NaOH溶液分别加水稀释,请在答题卷的图中画出两溶液的pH随体积稀释倍数的变化曲线(加必要标注)。
【答案】(1)108(2分)(2)1×10-13(2分)>(1分)(3)1∶9(3分)
(4)(3分)
【解析】
试题分析:(1)常温下,将1 mL pH=1的H2SO4溶液加水稀释到100 mL,稀释后的溶液中氢离子浓度是0.001mol/L,则根据水的离子积常数可知氢氧根的浓度是10-11mol/L,则![]() 。
。
(2) 某温度时,测得0.01 mol·L-1的NaOH溶液的pH=11,溶液中氢氧根的浓度是0.01mol/L,所以该温度下水的离子积常数KW=10-11×0.01=1×10-13。水的电离吸热,因此该温度>25 ℃。
(3) 在(2)所述温度下,将pH=12的NaOH溶液Va L与pH=2的硫酸Vb L混合。若所得混合液的pH=10,则![]() ,解得Va∶Vb=1∶9。
,解得Va∶Vb=1∶9。
(4)一水合氨是一元弱碱,存在电离平衡,稀释促进电离。氢氧化钠是强碱,完全电离,则将1mL pH均为11的氨水与NaOH溶液分别加水稀释后氢氧化钠的pH变化大,其图像为(间答案)。

【题目】下列各组反应(表内物质均为反应物)刚开始时,放出H2的速率最大的是( )
编号 | 金属(粉末状) | 物质的量 | 酸的浓度 | 酸的体积 | 反应温度 |
A | Mg | 0.1mol | 6mol/L硝酸 | 10mL | 60℃ |
B | Mg | 0.1mol | 3mol/L盐酸 | 10mL | 30℃ |
C | Fe | 0.1mol | 3mol/L盐酸 | 10mL | 60℃ |
D | Mg | 0.1mol | 3mol/L盐酸 | 10mL | 60℃ |
A.A
B.B
C.C
D.D
【题目】硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,在循环过程中价态变化在-2价至+6价之间,以不同的状态(或形态)发生一系列的变化,请分析此图并回答有关问题,
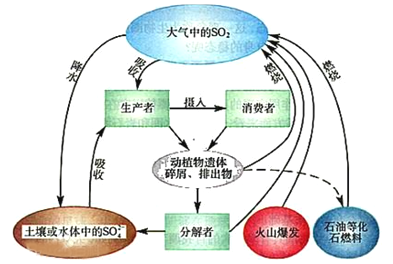
(1)硫循环与氮循环是自然界中两种重要的元素循环过程,下列关于这两种循环的说法正确的是_____
选项 | 比较 | 氮循环 | 硫循环 |
A | 异 | 氮元素会进入大气 | 硫元素不会进入大气 |
B | 碳循环过程有生物圈参与 | 硫循环过程无生物圈参与 | |
C | 同 | 人类活动对氮循环和硫循环都造成巨大影响 | |
D | 氮循环和硫循环对环境的影响是都能导致温室效应 | ||
(2)分解者可将含硫有机物分解为硫化氢,硫黄细菌和硫化细菌可将硫化氢进一步转变为元素硫或硫酸盐,下列关于硫化氢说法正确的是 _____________
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢是一种无色臭鸡蛋气味的有毒气体
(3)硫化氢虽然有毒,但有研究发现人体心肺血管中存在微量硫化氢,它对调节心血管功能具有重要作用,请再举出一例类似硫化氢“亦正亦邪”物质的实证______________________。
(4)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在较小,其原因可能是_____________________。(用化学方程式表示)
(5)研究发现,空气其中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不符的是___________(多选)
A.潮湿的氯气通过盛有浓H2SO4的洗气瓶
B.硫化氢通入浓H2SO4中
C.浓H2SO4滴入萤石中,加热
D.向盐酸中加入浓硫酸产生白雾
(6)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是_______。

(7)若采用如图所示的流程处理则气体a是_______________,Y一定含有______________。(填化学式)