题目内容
(2012?长沙模拟)设NA代表阿伏加德罗常数NA的数值,下列说法正确的是( )
分析:A、1mol氯酸钾中含有1mol硫酸根离子,含有2mol负电荷;
B、根据乙烯和环丙烷的最简式CH2计算出混合气体的物质的量及氢原子个数;
C、根据铁离子在溶液中发生水解数目会减少分析;
D、根据氯气的物质的量计算出反应转移的电子的物质的量及数目.
B、根据乙烯和环丙烷的最简式CH2计算出混合气体的物质的量及氢原子个数;
C、根据铁离子在溶液中发生水解数目会减少分析;
D、根据氯气的物质的量计算出反应转移的电子的物质的量及数目.
解答:解:A、1mol硫酸钾中阴离子为硫酸根离子,物质的量为1mol,1mol硫酸根离子带有2mol负电荷,所带电荷数为2NA,故A错误;
B、乙烯和环丙烷的最简式为CH2,24g混合气体中含有2molCH2,含有4mol氢原子,28g混合气体中含有4NA个氢原子,故B错误;
C、0.1mol氯化铁中含有0.1mol铁离子,由于三价铁离子发生了水解,溶液中三价铁离子的物质的量减小,所得溶液含有的三价铁离子数目小于0.1NA,故C错误;
D、标况下,22.4L氯气的物质的量为1mol,与氢氧化钠溶液完全反应,转移的电子的物质的量为1mol,转移的电子数为NA,故D正确;
故选:D.
B、乙烯和环丙烷的最简式为CH2,24g混合气体中含有2molCH2,含有4mol氢原子,28g混合气体中含有4NA个氢原子,故B错误;
C、0.1mol氯化铁中含有0.1mol铁离子,由于三价铁离子发生了水解,溶液中三价铁离子的物质的量减小,所得溶液含有的三价铁离子数目小于0.1NA,故C错误;
D、标况下,22.4L氯气的物质的量为1mol,与氢氧化钠溶液完全反应,转移的电子的物质的量为1mol,转移的电子数为NA,故D正确;
故选:D.
点评:本题考查了阿伏伽德罗常数,注意乙烯和丙烷的最简式相同,可以根据最简式计算含有的粒子数目,本题难度不大.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
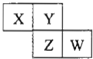 (2012?长沙模拟)X、Y、Z、W均为短周期元素,在周期表中位置如图所示.Y原子的最外层电子数是电子层数的3倍.下列说法中不正确的是( )
(2012?长沙模拟)X、Y、Z、W均为短周期元素,在周期表中位置如图所示.Y原子的最外层电子数是电子层数的3倍.下列说法中不正确的是( ) (2012?长沙模拟)某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验.
(2012?长沙模拟)某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验.