题目内容
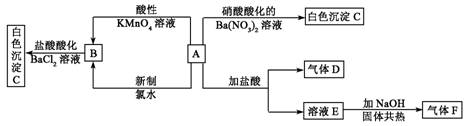
一种白色晶体A极易溶于水,将A配成溶液进行实验,实验现象及转化关系如下列框图所示:

其中A为正盐,气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝.试回答下列问题:
(1)写出下列物质化学式:A:______;C:______;
(2)写出下列反应的离子方程式:
①溶液E和氢氧化钠固体共热:______.
②A和新制氯水:______.
(3)请设计实验,依次证明某钠盐溶液中含有SO32-、SO42-、Cl-:______.
解:能使品红溶液褪色的是二氧化硫,所以D是二氧化硫,能使湿润的红色石蕊试纸变蓝的是氨气,即F是氨气,A是一种白色晶体,和其他物质反应既能生成氨气又能生成二氧化硫,所以A是(NH4)2SO3,容易被氧化剂氧化为硫酸铵,所以B是硫酸铵,得出E是氯化铵,白色沉淀C是硫酸钡,
(1)能和其他物质反应既能生成氨气又能生成二氧化硫的白色晶体是(NH4)2SO3,硫酸铵和氯化钡发生复分解反应生成硫酸钡沉淀,所以C是BaSO4,故答案为:(NH4)2SO3;BaSO4;
(2)①铵盐和强碱共热会生成氨气,是一种碱性气体,原理为NH4++OH- NH3↑+H2O,
NH3↑+H2O,
故答案为:NH4++OH- NH3↑+H2O;
NH3↑+H2O;
②氯气具有强氧化性,可与具有还原性的发生氧化还原反应,反应的离子方程式为Cl2+H2O+SO32-=SO42-+2H++2Cl-,
故答案为:Cl2+H2O+SO32-=SO42-+2H++2Cl-;
(3)检验SO32-和SO42-,可加入Ba(OH)2,过滤得到的沉淀中加入盐酸,如沉淀部分溶解,说明含有SO32-和SO42-,然后再向滤液中加入过量的稀硝酸,再加入硝酸银溶液,如得到白色沉淀,说明溶液中含有Cl-,注意在确定溶液中不含Ag+等干扰离子存在时可选用盐酸酸化的BaCl2溶液作试剂检验SO42-,在确定溶液中不含SO32-等干扰离子存在时可选用HNO3酸化的Ba(NO3)2溶液作试剂检验SO42-,
故答案为:可加入Ba(OH)2,过滤得到的沉淀中加入盐酸,如沉淀部分溶解,说明含有SO32-和SO42-,然后再向滤液中加入过量的稀硝酸,再加入硝酸银溶液,如得到白色沉淀,说明溶液中含有Cl-.
分析:能使品红溶液褪色的是二氧化硫,所以D是二氧化硫,能使湿润的红色石蕊试纸变蓝的是氨气,即F是氨气,A是一种白色晶体,和其他物质反应既能生成氨气又能生成二氧化硫,所以A是(NH4)2SO3,容易被氧化剂氧化为硫酸铵,所以B是硫酸铵,得出E是氯化铵,白色沉淀C是硫酸钡,结合物质的性质可解答该题.
点评:本题是一道框图推断题,注意寻找解题的突破口是关键,主要考查物质的性质,难度不大,解答本题时注意把握离子的检验方案的实验设计.
(1)能和其他物质反应既能生成氨气又能生成二氧化硫的白色晶体是(NH4)2SO3,硫酸铵和氯化钡发生复分解反应生成硫酸钡沉淀,所以C是BaSO4,故答案为:(NH4)2SO3;BaSO4;
(2)①铵盐和强碱共热会生成氨气,是一种碱性气体,原理为NH4++OH-
 NH3↑+H2O,
NH3↑+H2O,故答案为:NH4++OH-
 NH3↑+H2O;
NH3↑+H2O;②氯气具有强氧化性,可与具有还原性的发生氧化还原反应,反应的离子方程式为Cl2+H2O+SO32-=SO42-+2H++2Cl-,
故答案为:Cl2+H2O+SO32-=SO42-+2H++2Cl-;
(3)检验SO32-和SO42-,可加入Ba(OH)2,过滤得到的沉淀中加入盐酸,如沉淀部分溶解,说明含有SO32-和SO42-,然后再向滤液中加入过量的稀硝酸,再加入硝酸银溶液,如得到白色沉淀,说明溶液中含有Cl-,注意在确定溶液中不含Ag+等干扰离子存在时可选用盐酸酸化的BaCl2溶液作试剂检验SO42-,在确定溶液中不含SO32-等干扰离子存在时可选用HNO3酸化的Ba(NO3)2溶液作试剂检验SO42-,
故答案为:可加入Ba(OH)2,过滤得到的沉淀中加入盐酸,如沉淀部分溶解,说明含有SO32-和SO42-,然后再向滤液中加入过量的稀硝酸,再加入硝酸银溶液,如得到白色沉淀,说明溶液中含有Cl-.
分析:能使品红溶液褪色的是二氧化硫,所以D是二氧化硫,能使湿润的红色石蕊试纸变蓝的是氨气,即F是氨气,A是一种白色晶体,和其他物质反应既能生成氨气又能生成二氧化硫,所以A是(NH4)2SO3,容易被氧化剂氧化为硫酸铵,所以B是硫酸铵,得出E是氯化铵,白色沉淀C是硫酸钡,结合物质的性质可解答该题.
点评:本题是一道框图推断题,注意寻找解题的突破口是关键,主要考查物质的性质,难度不大,解答本题时注意把握离子的检验方案的实验设计.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
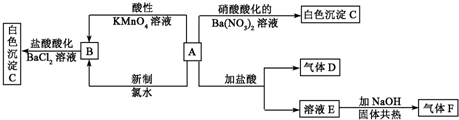
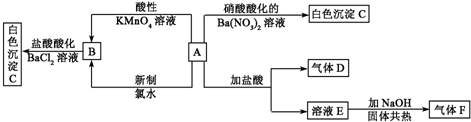
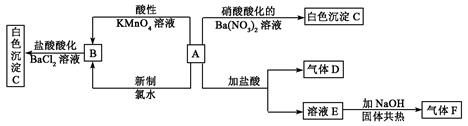
 写出下列物质化学式:A:_________________;C:_________________;
写出下列物质化学式:A:_________________;C:_________________; 离子方程式:
离子方程式: