��Ŀ����
����Ŀ��ʵ����������CoCl2��6H2OΪԭ����ȡ���Ȼ��������ܵ�ʵ�鲽�����£�
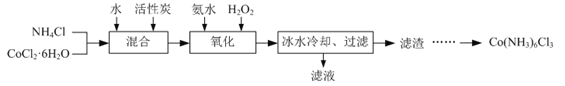
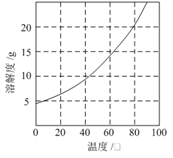
��֪����Co(NH3)6Cl3�ڲ�ͬ�¶���ˮ�е��ܽ����������ͼ��
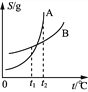
����Co(NH3)6Cl3��Һ�м���һ�������������ڽᾧ��
��Ksp=1.09��10-15��Ksp=2��10-44��
����ʵ�������NH4Cl������Ӧ���⣬���ɷ�ֹ�ڵμӰ�ˮʱc(OH-)������ԭ����___________��
�����������м��백ˮ��H2O2����Һ������Co(NH3)6Cl3��
������ʱ���ȼ��백ˮ�ټ���H2O2����ԭ����___________��
���÷�Ӧ�Ļ�ѧ����ʽΪ___________��
����Ӧʱ��Ҫ���Ʒ�Ӧ�¶���50 ��~60 ��֮�䣬�ɲ�ȡ�ļ��ȷ�ʽ��___________��
����ˮ��ȴ��Ŀ����___________��
���벹�������ɹ��˺�����������ȡCo(NH3)6Cl3��ʵ�鷽���������������ˮ�У���ֽ��裬
___________�����¸����ʵ������ʹ�õ��Լ������ᡢ�Ҵ���
���𰸡� NH4Cl����ˮ�����NH4+������NH3��H2O�ĵ��� ��ֹCo(OH)3������ H2O2+ 2CoCl2+2NH4Cl+10NH3��H2O��2Co(NH3)6Cl3+ 12H2O
��H2O2+ 2CoCl2+2NH4Cl+10NH3��2Co(NH3)6Cl3+ 2H2O ˮԡ���� �������Ȼ��������ܵ��ܽ�ȣ���߲��� ���ȹ��ˣ�����Һ�м�������Ũ���ᣬ�ñ�ˮԡ��ȴ����ˣ����������Ҵ�ϴ��
����������1���ڼ������������������������ܳ��������ԭ��NH4Cl����Ҫ���ó����ṩNH3���⣬NH4Cl����ˮ�����NH4+������NH3H2O�ĵ��룬������Һ�ļ��ԣ�
��2��������ʱ���ȼ��백ˮ�ټ���H2O2�����ȼӹ������⣬��+2����������+3�ۣ��ټ��백ˮ������Co��OH��3�����ɣ������ڲ�������ɣ�
�����������м��백ˮ��H2O2����Һ������Co��NH3��6Cl3�ķ�Ӧ��Ϊ��H2O2+2CoCl2+2NH4Cl+10NH3H2O=2Co��NH3��6Cl3+12H2O��H2O2+2CoCl2+2NH4Cl+10NH3=2Co��NH3��6Cl3+2H2O��
����ˮԡ���ȿ��Ʒ�Ӧ�¶���50����60��֮�䣻
��3����ͼ2��֪Co��NH3��6Cl3ˮ�е��ܽ�����¶ȵ����߶�������Ϊ�˽������Ȼ��������ܵ��ܽ�ȣ���߲�����Ӧ��ˮ��ȴ��
��4���ɹ��˺�����������ȡCo��NH3��6Cl3��ʵ�鷽���������������ˮ�У���ֽ��裬���ȹ��ˣ�����Һ�м�������Ũ���ᣬ�ñ�ˮԡ��ȴ����ˣ����������Ҵ�ϴ�ӡ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�