题目内容
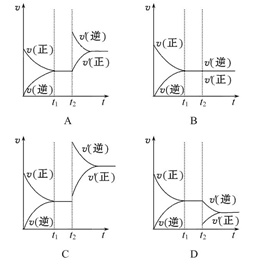
在密闭容器中,通入2 mol SO2和1 mol O2,发生反应2SO2+O2 2SO3,在t1时刻达到平衡。保持其他条件不变,在t2时刻,再通入一定量的SO3,下列有关反应速率(v)与时间(t)的关系曲线正确的是( )
2SO3,在t1时刻达到平衡。保持其他条件不变,在t2时刻,再通入一定量的SO3,下列有关反应速率(v)与时间(t)的关系曲线正确的是( )
 2SO3,在t1时刻达到平衡。保持其他条件不变,在t2时刻,再通入一定量的SO3,下列有关反应速率(v)与时间(t)的关系曲线正确的是( )
2SO3,在t1时刻达到平衡。保持其他条件不变,在t2时刻,再通入一定量的SO3,下列有关反应速率(v)与时间(t)的关系曲线正确的是( )
A
反应达到平衡时,增大SO3的浓度,瞬间逆反应速率增大,正反应速率不变,故A项正确。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 2C(g) ΔH<0 的正确图像是下图中的( )
2C(g) ΔH<0 的正确图像是下图中的( )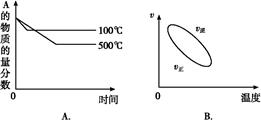
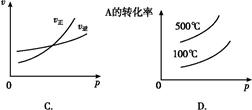
 2NH3。
2NH3。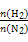 表示起始时H2和N2的物质的量之比,且起始时H2和N2的物质的量之和相等。下列图像正确的是( )
表示起始时H2和N2的物质的量之比,且起始时H2和N2的物质的量之和相等。下列图像正确的是( )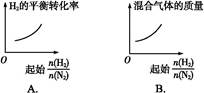
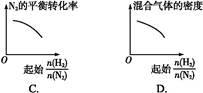
 CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
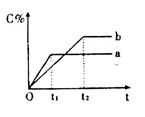
CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )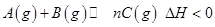 ,在不同条件下反应混合物中C的百分含量反应过程所需时间的关系曲线。下列有关叙述正确的是
,在不同条件下反应混合物中C的百分含量反应过程所需时间的关系曲线。下列有关叙述正确的是