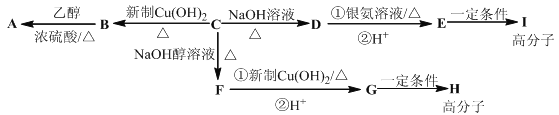题目内容
【题目】甲烷、乙烯、乙醇、乙酸都是常见的有机物,下列说法正确的是
A. 甲烷中混有乙烯,用酸性高锰酸钾溶液除去
B. 乙醇不能使酸性高锰酸钾溶液褪色
C. 酒越陈越香与酯化反应有关
D. 乙醇与乙酸酯化反应时用稀硫酸作催化剂
【答案】C
【解析】A、乙烯被酸性高锰酸钾氧化为CO2,除去乙烯的同时会引入新的气体杂质,故A错误;B、乙醇能被酸性高锰酸钾氧化为乙酸,则乙醇能使酸性高锰酸钾褪色,故B错误;C、酒中含乙醇,久置后的乙醇可能被氧化成乙酸,乙醇和乙酸在一定条件下反应生成具有香味的乙酸乙酯,所以酒是陈的香,故C正确;D、乙醇与乙酸酯化时应用浓硫酸作催化剂和吸水剂,乙酸乙酯水解可选用稀硫酸做催化剂,故D错误。故选C。

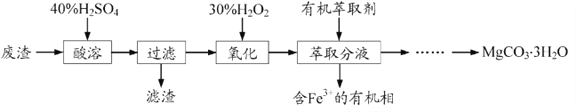
【题目】某小组同学做“硫在氧气中燃烧”的实验时,老师建议在集气瓶底部放少量NaOH溶液吸收生成的SO2。这种做法引起了同学们的思考:SO2与NaOH是否发生反应。
【查阅资料】通常状况下,1体积水约能溶解40体积SO2。
【实验方案】同学们向充满SO2的软塑料瓶中迅速倒入一定量NaOH溶液,拧紧瓶盖,振荡,发现塑
料瓶变瘪,他们认为SO2与NaOH发生了反应。
【反思与改进】甲同学认为上述实验不够严谨,理由是_________________。于是同学们设计了如下两
个改进方案。
方案一:
实验操作 | 实验现象 |
向两个充满SO2的200 mL软塑料瓶中分别注入10 mL水和NaOH溶液,振荡,对比。 | 两个瓶子变瘪的程度完全相同 |
乙同学认为由于两个瓶子变瘪的程度完全相同,因此无法证明SO2与NaOH是否发生了反应。试分析导致两个瓶子变瘪的程度完全相同的原因是_____________________。他认为若改变注入水和NaOH溶液的体积便可达到实验目的,注入液体的体积可以是__________(填序号)。
a.15 mL b.8 mL c.5 mL d.3 mL
方案二:
实验操作 | 实验现象 |
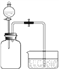
利用如图所示装置进行实验: 向两个充满SO2的300 mL集气瓶 中分别加入6 mL水和NaOH溶液, 一段时间后,打开止水夹,对比。
| 倒吸入两个集气瓶中的液体体积完全相同 |
丙同学认为上述方案也无法证明SO2与NaOH是否发生反应。你认为导致吸入液体的体积完全相同的原因是___________________。
丁同学思考后,将上述装置进行了改进,便达到实验目的。改进装置如下图所示,你认为装置B的作用是_______________。