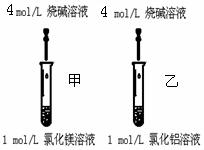
题目内容
| |||||||||||||||
答案:
解析:
解析:
(1) |
AG(或AGE),2H2O2 |
(2) |
BG(或BGE),2KBr+2H2SO4(浓)+MnO2 |
(3) |
①倒置的漏斗可以防止HBr溶于水产生倒吸(1分);橡破塞孔4接10端,是为了利用长导管起冷凝回流作用(1分);②NaOH溶液(或其他碱溶液)(1分);分液漏斗(多填其他合理仪器不扣分)(1分). |

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目