题目内容
所含分子数相同的一组物质是
- A.1gH2和1gN2
- B.1molH2O和1gH2O
- C.3.2gO2和4.8gO3
- D.44gCO2和16gO2
C
分析:物质的量相同,所含分子数目相同,根据n= 计算判断.
计算判断.
解答:A、1gH2和1gN2,二者物质的量之比与摩尔质量成反比为28:2=14:1,故二者含有分子数之比为14:1,不相等,故A错误;
B、1gH2O的物质的量为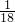 mol,二者物质的量不同,含有水分子数目不同,故B错误;
mol,二者物质的量不同,含有水分子数目不同,故B错误;
C、3.2gO2的物质的量为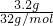 =0.1mol,4.8gO3的物质的量为
=0.1mol,4.8gO3的物质的量为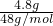 =0.1mol,二者物质的量相同,含有相同的分子数目,故C正确;
=0.1mol,二者物质的量相同,含有相同的分子数目,故C正确;
D、44gCO2的物质的量为1mol,16gO2的物质的量为0.5mol,二者物质的量不同,含有的分子数目不同,故D错误;
故选C.
点评:本题考查物质的量的有关计算,比较基础,旨在考查学生对基础知识的理解掌握,注意对公式的理解与灵活运用.
分析:物质的量相同,所含分子数目相同,根据n=
 计算判断.
计算判断.解答:A、1gH2和1gN2,二者物质的量之比与摩尔质量成反比为28:2=14:1,故二者含有分子数之比为14:1,不相等,故A错误;
B、1gH2O的物质的量为
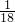 mol,二者物质的量不同,含有水分子数目不同,故B错误;
mol,二者物质的量不同,含有水分子数目不同,故B错误;C、3.2gO2的物质的量为
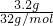 =0.1mol,4.8gO3的物质的量为
=0.1mol,4.8gO3的物质的量为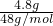 =0.1mol,二者物质的量相同,含有相同的分子数目,故C正确;
=0.1mol,二者物质的量相同,含有相同的分子数目,故C正确;D、44gCO2的物质的量为1mol,16gO2的物质的量为0.5mol,二者物质的量不同,含有的分子数目不同,故D错误;
故选C.
点评:本题考查物质的量的有关计算,比较基础,旨在考查学生对基础知识的理解掌握,注意对公式的理解与灵活运用.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目