题目内容
Cl2通入70℃的某浓度的氢氧化钠水溶液中,能同时发生两个自身氧化还原反应(未配平):NaOH + Cl2 → NaCl + NaClO + H2O,NaOH + Cl2 → NaCl + NaClO3 + H2O。反应完成后测得溶液中NaClO与NaClO3的数目之比为5:2,则该溶液中NaCl与NaClO的数目之比为
| A.3∶1 | B.2∶1 | C.15∶2 | D.1∶1 |
A
试题分析:设溶液中NaClO与NaClO3的物质的量分别为5mol、2mol,NaClO与NaClO3均是氯气的氧化产物,转移电子的物质的量=5mol×1+2mol×(5-0)=15mol。氯气的还原产物是氯化钠,则根据电子注意守恒可知NaCl的物质的量=5mol×1+2mol×(5-0)=15mol,因此该溶液中NaCl与NaClO的数目之比为15mol:5mol=3:1,答案选A。

练习册系列答案
相关题目
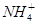 离子中的键角
离子中的键角