题目内容
化学反应常常伴随能量的变化,以下是H2与Cl2反应的能量变化示意图H2 (g) +Cl2 (g)=2HCl(g)反应的能量变化示意图,下列说法正确的是( )

A. 氯化氢分子的电子式: B. 该反应是工业制取盐酸的化学反应原理
B. 该反应是工业制取盐酸的化学反应原理
C. 形成1molH—Cl键要吸收431kJ的能量 D. 该反应中反应物总能量小于生成物总能量
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案环己烯是一种重要的化工原料。
(1)实验室可由环己醇制备环己烯,反应的化学方程式是______________________________________________________。
(2)实验装置如下图所示,将10 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
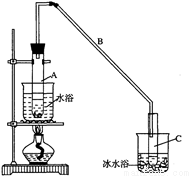
环己醇和环己烯的部分物理性质如下:
密度 | 熔点 | 沸点 | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
① A中碎瓷片的作用是_____________;导管B除了导气外还具有的作用是___________________。
② 试管A置于水浴中的目的是_________________________________;
试管C置于冰水浴中的目的是_______________________________。
(3)环己烯粗品中含有少量环己醇和酸性杂质。精制环己烯的方法是:
① 向环己烯粗品中加入_________(填入编号),充分振荡后,___________________(填操作名称)。
A.Br2的CCl4溶液 B.稀H2SO4 C.Na2CO3溶液
② 再对初步除杂后的环己烯进行蒸馏,得到环己烯精品。蒸馏时,蒸馏烧瓶中要加入少量生石灰,目的是__________________________。
③ 实验制得的环己烯精品质量低于理论产量,可能的原因是_______________。
A.蒸馏时从70℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(4)以下区分环己烯精品和粗品的方法,合理的是________________。
A.加入水观察实验现象
B.加入金属钠观察实验现象
C.加入酸性高锰酸钾溶液,振荡后观察实验现象


 得电子能力相同
得电子能力相同