题目内容
a、b、c、d、e、f、g为七种由短期周期元素构成的粒子,它们都有10个电子,其结构特点如下:
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;c与f反应可形成两个g分子。试写出:
(1)a粒子的核外电子排布式______________________________。
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱为:________>________ (用化学式表示)。
(3)d溶于水的电离方程式__________________________________________。
(4)c粒子是__________,f粒子是__________(用化学式表示)。
(5)g粒子的共价键数是_____而不是更多,说明共价键具有 性。
| 粒子代码 | a | b | c | d | e | f | g |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 电荷数(单位电荷) | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;c与f反应可形成两个g分子。试写出:
(1)a粒子的核外电子排布式______________________________。
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱为:________>________ (用化学式表示)。
(3)d溶于水的电离方程式__________________________________________。
(4)c粒子是__________,f粒子是__________(用化学式表示)。
(5)g粒子的共价键数是_____而不是更多,说明共价键具有 性。
(7分)(每空1分)(1)1s22s22p6 (2)NaOH Mg(OH)2
(3)NH3+H2O NH3·H2O
NH3·H2O NH+4+OH- (4)OH- H3O+?(5)2 饱和性
NH+4+OH- (4)OH- H3O+?(5)2 饱和性
(3)NH3+H2O
 NH3·H2O
NH3·H2O NH+4+OH- (4)OH- H3O+?(5)2 饱和性
NH+4+OH- (4)OH- H3O+?(5)2 饱和性试题分析:(1)a粒子是单核10电子微粒,所以a是Ne,则根据构造原理可知核外电子排布式为1s22s22p6。
(2)b是单核带一个正电荷10电子微粒,则b是钠离子。e是双核带一个正电荷10电子微粒,则e是镁离子。金属性是钠强于镁,金属性越强,最高价氧化物对应水化物的碱性越强。所以b与e相应元素的最高价氧化物对应水化物的碱性强弱为:NaOH>Mg(OH)2。
(3)d是多核10电子分子,且d是由极性键构成的四原子分子,则d是氨气。所以氨气溶于水的电离方程式为NH3+H2O
 NH3·H2O
NH3·H2O NH+4+OH-。
NH+4+OH-。(4)c是双核带一个副电荷10电子微粒,则c是OH-。f是多核带一个正电荷10电子微粒,且c与f反应可形成两个g分子,其中g是多核10电子分子,因此符合条件是的OH-+H3O+=2 H2O,即c是OH-,f是H3O+。
(5)水分子中含有2个O-H极性键,即共价键数是2个而不是更多,说明共价键具有饱和性。

练习册系列答案
相关题目
 ,其基态原子的价电子层电子排布式正确的是
,其基态原子的价电子层电子排布式正确的是
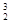 He。关于
He。关于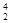 He互为同位素
He互为同位素