题目内容
【题目】下列关于化学键的叙述正确的是
A. 离子化合物一定不含共价键
B. 化学键的形成与原子结构无关
C. 化学键主要通过原子的价电子间的转移或共用来实现
D. 离子键可能存在于共价化合物中
【答案】C
【解析】
A.离子化合物中可能含有共价键,如NaOH、KHS等,故A错误;
B.化学键的形成与原子结构有关,若原子半径越大,最外层电子数越少,越易失电子而形成离子键,故B错误;
C.化学键主要通过原子的价电子间的转移或共用来实现,故C正确;
D.共价化合物中只含有共价键,不可能含有离子键,故D错误;
答案选C。

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案【题目】Ⅰ.煤是一种重要的化工原料,人们将利用煤制取的水煤气、焦炭、二甲醚等广泛用于工农业生产中.已知: C(s)+H2O(g)═CO(g)+H2(g) △H=+131.3kJmol﹣1
CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41.3kJmol﹣1
则炭与水蒸气反应生成二氧化碳和氢气的热化学方程式为___________________。该反应在____(填“高温”、“低温”或“任何温度”)下有利于正向自发进行.
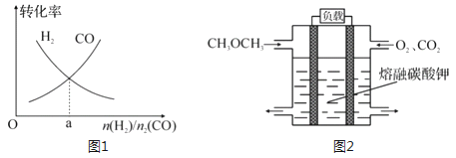
Ⅱ.二甲醚(CH3OCH3)被誉为“21世纪的清洁燃料”。 利用煤制取的CO和H2为原料生产二甲醚主要发生以下三个反应:① CO(g)+2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
② 2CH3OH(g)![]() CH3OCH3(g)+H2O(g)△H2=﹣24kJmol﹣1
CH3OCH3(g)+H2O(g)△H2=﹣24kJmol﹣1
③CO(g)+H2O(g)![]() CO2(g)+H2(g)△H3=﹣41kJmol﹣1
CO2(g)+H2(g)△H3=﹣41kJmol﹣1
(1)已知反应①中的相关的化学键键能数据如下:
化学键 | H﹣H | C﹣O |
| H﹣O | C﹣H |
E/(kJ·mol﹣1) | 436 | 343 | 1076 | 465 | 413 |
由上述数据计算△H1=______________;
(2)该工艺的总反应为3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g)△H,该反应
CH3OCH3(g)+CO2(g)△H,该反应
△H=____________,
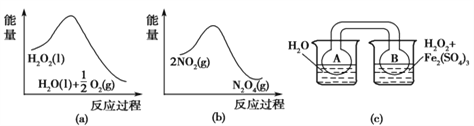
Ⅲ.在固定体积的密闭容器中,发生可逆反应:2NO2(g) ![]() N2O4(g)。已知Fe3+对H2O2的分解具有催化作用。利用下图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的________(填“深”或“浅”),其原因是____________________________
N2O4(g)。已知Fe3+对H2O2的分解具有催化作用。利用下图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的________(填“深”或“浅”),其原因是____________________________