题目内容
由两种金属组成的混合物12 g,与足量的稀硫酸反应后,在标准状况下产生H2为11.2升,这种金属混合物可能是( )
| A.Na与Mg | B.Fe与Zn | C.Al与Cu | D.Mg与Zn |
C
标准状况下11.2升氢气的物质的量为0.5mol,由方程式: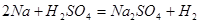 ;
;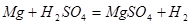 ;
;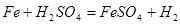 ;
;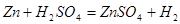 ;
;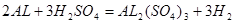 ;可知若氢气全部由钠生成,则需钠的质量为23克;若氢气全部由镁生成,则需镁的质量为12克;若氢气全部由铁生成,则需铁的质量为28克;若氢气全部由锌生成,则需锌的质量为32.5克;若全部由铝生成,则需铝的质量为9克;所以由两种金属组成的混合物12 g,与足量的稀硫酸反应后,在标准状况下产生H2为11.2升,这种金属混合物的正确选项只能是C;
;可知若氢气全部由钠生成,则需钠的质量为23克;若氢气全部由镁生成,则需镁的质量为12克;若氢气全部由铁生成,则需铁的质量为28克;若氢气全部由锌生成,则需锌的质量为32.5克;若全部由铝生成,则需铝的质量为9克;所以由两种金属组成的混合物12 g,与足量的稀硫酸反应后,在标准状况下产生H2为11.2升,这种金属混合物的正确选项只能是C;
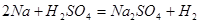 ;
;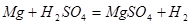 ;
;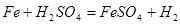 ;
;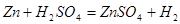 ;
;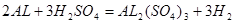 ;可知若氢气全部由钠生成,则需钠的质量为23克;若氢气全部由镁生成,则需镁的质量为12克;若氢气全部由铁生成,则需铁的质量为28克;若氢气全部由锌生成,则需锌的质量为32.5克;若全部由铝生成,则需铝的质量为9克;所以由两种金属组成的混合物12 g,与足量的稀硫酸反应后,在标准状况下产生H2为11.2升,这种金属混合物的正确选项只能是C;
;可知若氢气全部由钠生成,则需钠的质量为23克;若氢气全部由镁生成,则需镁的质量为12克;若氢气全部由铁生成,则需铁的质量为28克;若氢气全部由锌生成,则需锌的质量为32.5克;若全部由铝生成,则需铝的质量为9克;所以由两种金属组成的混合物12 g,与足量的稀硫酸反应后,在标准状况下产生H2为11.2升,这种金属混合物的正确选项只能是C;
练习册系列答案
相关题目
 80多种工业以汞为原料,生产过程中产生的汞的污染越来越引起人们
80多种工业以汞为原料,生产过程中产生的汞的污染越来越引起人们 的重视,水体中的无机汞主要有Hg2+、Hg22+。
的重视,水体中的无机汞主要有Hg2+、Hg22+。 +可用KI及CuSO4溶液与其反应生成橙红色Cu2HgI4沉淀,用漫反射光谱直接测定汞沉淀物,该反应的离子方程式可表示为: 。
+可用KI及CuSO4溶液与其反应生成橙红色Cu2HgI4沉淀,用漫反射光谱直接测定汞沉淀物,该反应的离子方程式可表示为: 。 吸收总反应为:2Hg+SO2+8I一+4H+ =2HgI
吸收总反应为:2Hg+SO2+8I一+4H+ =2HgI +S+2H2O,最后进行电解吸收液(K2HgI4),阴极的电极反应式为: 。
+S+2H2O,最后进行电解吸收液(K2HgI4),阴极的电极反应式为: 。