题目内容
下图是一个制取氯气并以氯气为原料制取氯化铁的装置,请回答下列问题。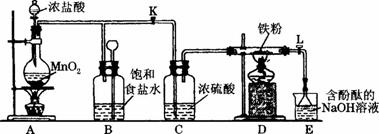
(1)A是氯气发生装置,其中发生的反应的离子方程式为_______________________________。
(2)实验开始时,先点燃装置A处的酒精灯,打开旋塞K、L,让Cl2充满整个装置,再点燃装置D处的酒精灯,Cl2通过C瓶后再进入D装置的硬质玻璃管,D中发生反应的化学方程式为__________________________________________________________________。
(3)装置C的作用是_______________________________________________________。
如果没有装置C,而让气体直接进入D,则D中反应产物将可能含杂质_________(填化学式)。
(4)D处反应完毕后,关闭旋塞K、L,移去酒精灯,由于余热的作用,装置A仍有Cl2产生,此时B中出现的现象是___________________________________________________________;
装置B的作用是_________________________________________________________。
(5)实验开始,E中溶液红色褪去,褪色的原因可能①溶液已变酸性,酚酞呈无色 ②酚酞被氧化褪色。
请没汁一个实验方案验证褪色的原因是①或②(简述实验操作、现象、结论)。
(1)MnO2+4H++![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)2Fe+![]() 2FeCl3
2FeCl3
(3)干燥氯气 Fe2O3(填Fe3O4也可)
(4)瓶中液面下降,长颈漏斗中液面上升;贮存少量多余的Cl2(其他合理答案也可)
(5)取少量E中已褪色的溶液,滴加浓NaOH溶液,若溶液变红说明褪色原因是①,否则是②(其他合理答案也可)

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案