题目内容
13.已知:断裂下列化学键需要吸收的能量分别为:H-H 436kJ/mol;F-F 153kJ/mol;H-F 565kJ/mol.下列说法正确的是( )| A. | H2与F2反应的热化学方程式为:H2(g)+F2(g)=2HF(g);△H=-541 kJ | |
| B. | 2 L HF气体分解成1 L H2和1 L F2吸收541 kJ的热量 | |
| C. | 在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 | |
| D. | 1 mol H2与1 mol F2反应生成2 mol液态HF放出热量小于541 kJ |
分析 A、反应热的单位为kJ/mol.根据反应热△H=反应物总键能-生成物总键能计算反应热,书写热化学方程式;
B、气体所处的状态不确定;
C、根据键能,判断反应是放热反应还是吸热反应,反应物的总能量高于生成物的总能量,反应为放热反应,反应物的总能量小于生成物的总能量,反应为吸热反应;D、同一物质气态的能量比液态的能量高,结合能量守恒判断.
解答 解:A、反应热的单位为kJ/mol,各化学键键能:H-H 436kJ/mol;F-F 153kJ/mol;H-F 565kJ/mol,所以对于反应H2(g)+F2(g)=2HF(g)的反应热为△H=436kJ/mol+153kJ/mol-2×565kJ/mol=-541kJ/mol,该反应的热化学方程式为于H2(g)+F2(g)=2HF(g)△H=-541kJ/mol,故A错误;
B、由A可知2molHF分解,吸收的热量为541kJ,气体所处的状态不确定,不清楚2L氟化氢的物质的量是多少,无法确定吸收热量,故B错误;
C、由A可知H2与F2反应生成HF为放热反应,所以在相同条件下,1molH2与1molF2的能量总和大于2molHF气体的能量,故C正确;
D、由A可知1molH2与1molF2反应生成2molHF(g),放出的热量为541kJ,液态HF的能量比气体HF的能量低,所以1molH2与1molF2反应生成2mol液态HF放出热量大于541kJ,故D错误;
故选C.
点评 本题考查热化学方程式的书写与意义、反应热与化学键及物质能量关系、物质状态与能量关系,难度不大,注意基础知识的理解与掌握.

练习册系列答案
相关题目
3.反应3A(g)+B(g)?2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是( )
| A. | v (D)=0.4 mol•L-1•s-1 | B. | v (C)=0.5 mol•L-1•s-1 | ||
| C. | v (B)=0.6 mol•L-1•s-1 | D. | v (A)=0.15 mol•L-1•s-1 |
4.下列说法不正确的是( )
| A. | 镁铝合金密度较小、强度高,常用作制造航天器的材料 | |
| B. | 能自发进行的化学反应,可能是△H>0、△S>0 | |
| C. | CaC2着火时可使用泡沫灭火器灭火 | |
| D. | 黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
1.下列物质间发生反应时,都有SO2生成的是:( )
①硫在空气中燃烧 ②含硫的化合物在空气中灼烧 ③亚硫酸钠和硫酸反应 ④硫化氢在空气中完全燃烧 ⑤铜和热浓硫酸反应.
①硫在空气中燃烧 ②含硫的化合物在空气中灼烧 ③亚硫酸钠和硫酸反应 ④硫化氢在空气中完全燃烧 ⑤铜和热浓硫酸反应.
| A. | 只有①③④ | B. | 只有①⑤ | C. | 只有①③④⑤ | D. | ①②③④⑤ |
18.下列说法你认为不合理的是( )
| A. | 使用一次性筷子,既方便又卫生,且耗木才不多、应提倡大量使用 | |
| B. | 塑料像把双刀剑,它既可极大地方便人们的生活,又给环境带来污染 | |
| C. | 甲烷是优良的气体燃料,但矿井里由于它的存在,在通风不良时,易发生爆炸 | |
| D. | 大气中CO2的浓度不断上升,使全球变暖,但同时也有利于植物光合作用 |
5.下列表示物质结构的化学用语或模型正确的是( )
| A. | 乙烯的结构简式为CH2CH2 | B. | CH4分子的球棍模型: | ||
| C. | 醛基的电子式: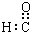 | D. | 葡萄糖的最简式(实验式):CH2O |
2.毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2•2H2O的流程如下:
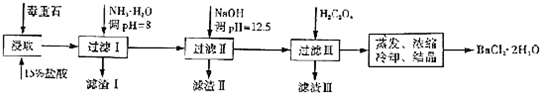
(1)毒重石用盐酸浸取前需充分研磨,目的是增大接触面积从而使反应速率加快.实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的ac.
a.烧杯 b.容量瓶 c.玻璃棒 d.滴定管
(2)
加入NH3•H2O调节pH=8可除去Fe3+(填离子符号),滤渣Ⅱ中含Mg(OH)2、Ca(OH)2(填化学式).加入H2C2O4时应避免过量,原因是H2C2O4过量会导致生成BaC2O4沉淀,产品的产量减少.
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行.
已知:2CrO42-+2H+═Cr2O72-+H2O Ba2++CrO42-═BaCrO4↓
步骤Ⅰ移取xml一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL.
步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL.则BaCl2溶液的浓度为$\frac{({V}_{0}-{V}_{1})b}{y}$mol•L-1.

(1)毒重石用盐酸浸取前需充分研磨,目的是增大接触面积从而使反应速率加快.实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的ac.
a.烧杯 b.容量瓶 c.玻璃棒 d.滴定管
(2)
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行.
已知:2CrO42-+2H+═Cr2O72-+H2O Ba2++CrO42-═BaCrO4↓
步骤Ⅰ移取xml一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL.
步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL.则BaCl2溶液的浓度为$\frac{({V}_{0}-{V}_{1})b}{y}$mol•L-1.
3.与普通玻璃相比具有相同组成的是( )
| A. | 钢化玻璃 | B. | 光学玻璃 | C. | 石英玻璃 | D. | 有色玻璃 |