题目内容
将11.5 g金属钠投入到88.5 g水中,反应完毕后,求生成溶液的质量分数(不考虑水的蒸发)。
生成NaOH溶液的质量分数为20.1%。
本题的解题关键是弄清钠跟水反应有氢气产生,所得溶液中的溶质是NaOH。
设消耗水的质量为x,生成NaOH和H2的质量分别为y、z,则:
2Na + 2H2O====2NaOH+H2↑
46 36 80 2
11.5 g x y z
46∶36="11.5" g∶x x="9" g
46∶80="11.5" g∶y y="20" g
46∶2="11.5" g∶z z="0.5" g
解法1:w(NaOH)= ×100%=20.1%
×100%=20.1%
解法2:w(NaOH)=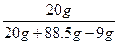 ×100%=20.1%
×100%=20.1%
设消耗水的质量为x,生成NaOH和H2的质量分别为y、z,则:
2Na + 2H2O====2NaOH+H2↑
46 36 80 2
11.5 g x y z
46∶36="11.5" g∶x x="9" g
46∶80="11.5" g∶y y="20" g
46∶2="11.5" g∶z z="0.5" g
解法1:w(NaOH)=
 ×100%=20.1%
×100%=20.1%解法2:w(NaOH)=
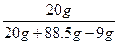 ×100%=20.1%
×100%=20.1%
练习册系列答案
相关题目

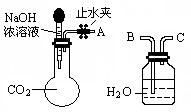
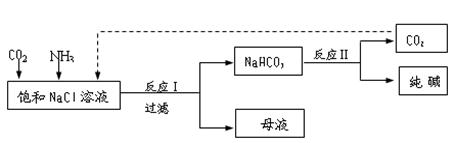
 NaHCO3↓+NH4Cl,处理母液的两种方法如下。
NaHCO3↓+NH4Cl,处理母液的两种方法如下。