题目内容
某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如下图所示(夹持仪器已略去)。

A B
(1)实验前,应先检查装置的 ;实验中产生的尾气应通入 溶液。
(2)实验过程中需要配制100mL1mol/L FeCl3溶液(未用浓盐酸酸化),所需要的玻璃仪器有:烧杯、量筒、胶头滴管、玻璃棒、 。
(3)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色,然后开始实验。
步骤① | 配制1 mol·L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1,取少量装 |
写出装置A中产生SO2的化学方程式: 。
(4)当SO2通 入到FeCl3溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象。将混合液放置12小时,溶液才变成浅绿色。
入到FeCl3溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象。将混合液放置12小时,溶液才变成浅绿色。
【查阅资料】 Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+。生成Fe(HSO3)2+离子的反应为可逆反应。
解释SO2与FeCl3溶液反应生成红棕色Fe(HSO3)2+离子的原因(用化学用语解释): 。
写出溶液中Fe(HSO3)2+离子与Fe3+反应的离子方程式:  。
。
(5)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学 进行了步骤③的实验。
进行了步骤③的实验。
步骤② | 往5mL1mol·L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色。微热3 min,溶 |
步骤③ | 往5mL重新配制的1mol·L-1 FeCl3溶液(用浓盐酸酸化)中通入SO |
⑹综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
II.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
III. 。
化学物质在生活中有着广泛的应用,下列对应关系错误的是
选项 | 性质 | 应用 |
A | 镁铝合金强度大、质量轻、抗腐蚀能力强 | 制造飞机 |
B | 晶体硅化学性质稳定,能导电 | 制造光纤 |
C | 稀硫酸能与Fe2O3反应 | 除去钢铁表面的铁锈 |
D | NaHCO3受热易分解 | 作焙制糕点的发酵粉 |


 二氯甲烷中含有的碳氯共价键的数目为0.2NA
二氯甲烷中含有的碳氯共价键的数目为0.2NA A.反应中硫酸作氧化剂 B.NH4CuSO3中硫元素被氧化
A.反应中硫酸作氧化剂 B.NH4CuSO3中硫元素被氧化
 B.Mg2+的结构示意图:
B.Mg2+的结构示意图:
 D.甲酸甲酯的结构简式:C2H4O2
D.甲酸甲酯的结构简式:C2H4O2 在一定条件下可以把Mn2+氧化成MnO
在一定条件下可以把Mn2+氧化成MnO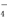 ,若反应中R2O
,若反应中R2O ,又知反应中氧化剂与还原剂的物质的量之比为5∶2,则n值为( )
,又知反应中氧化剂与还原剂的物质的量之比为5∶2,则n值为( ) 2CaO+O2↑+2xH2O,得到的O2在标准状况下体积为67.2ml.该样品中CaO2的物质的量为__________。
2CaO+O2↑+2xH2O,得到的O2在标准状况下体积为67.2ml.该样品中CaO2的物质的量为__________。 ,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70g.
,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70g.