题目内容
甲、乙、丙、丁均为中学化学常见的物质,它们之间的转化关系如下图(反应条件及其它产物已略去)。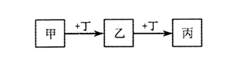
下列说法不正确的是
| A.若甲是AlCl3溶液,则丁可能是NaOH溶液 |
| B.若甲是Fe,则丁可能是Cl2 |
| C.若丁是CO2,则甲可能为Mg |
| D.若丁是O2,则乙、丙的相对分子质量可能相差16 |
B
解析试题分析:A.若甲是AlCl3溶液,向其中滴加少量的NaOH溶液时,发生反应:AlCl3+3NaOH=Al(OH)3↓+3NaCl;继续滴加时,会发生反应:Al(OH)3+NaOH=NaAlO2+2H2O。正确。B.若甲是Fe,则无论Cl2量的多少,都会发生反应:2Fe+ 3Cl2 2FeCl3;后边无法发生反应。错误。C.若丁是CO2,甲为Mg,会发生反应:2Mg+ CO2
2FeCl3;后边无法发生反应。错误。C.若丁是CO2,甲为Mg,会发生反应:2Mg+ CO2 2MgO+C;CO2过量时发生反应:CO2+C
2MgO+C;CO2过量时发生反应:CO2+C 2CO;正确。D.若甲是S,发生反应:S+ O2
2CO;正确。D.若甲是S,发生反应:S+ O2 SO2,2SO2+ O2
SO2,2SO2+ O2 2SO3;SO2、SO3的相对分子质量相差16。正确。
2SO3;SO2、SO3的相对分子质量相差16。正确。
考点:考查物质的性质及相互转化的知识。

 阅读快车系列答案
阅读快车系列答案下列物质性质与应用对应关系正确的是
| A.晶体硅熔点高硬度大,可用于制作半导体材料 |
| B.氢氧化铝具有弱碱性,可用于制胃酸中和剂 |
| C.漂白粉在空气中不稳定,可用于漂白纸张 |
| D.氧化铁能与酸反应,可用于制作红色涂料 |
下列药品和装置合理且能完成相应实验的是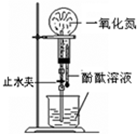
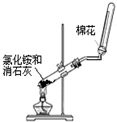
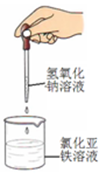
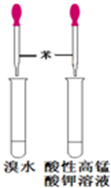
A B C D
| A.喷泉实验 | B.实验室制取并收集氨气 |
| C.制备氢氧化亚铁 | D.验证苯中是否含有碳碳双键 |
a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知:①a、c皆能与稀硫酸反应放出气体;②b与d的硝酸盐反应,置换出单质d;③c与强碱反应放出气体;④c、e在冷浓硫酸中发生钝化。由此可判断a、b、c、d、e依次为
| A.Fe Cu Al Ag Mg | B.Al Cu Mg Ag Fe |
| C.Mg Cu Al Ag Fe | D.Mg Ag Al Cu Fe |
下列有关物质的性质和该性质的应用均正确的是
| A.SiO2具有较好的导电性,可用于制造半导体材料 |
| B.H2O2是一种绿色氧化剂,可氧化酸性高锰酸钾而产生O2 |
| C.铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸 |
| D.Mg在空气中燃烧发出耀眼的白光,可用于制作信号弹 |
Cu、Cu2O和CuO组成的混合物加入100 mL 0.6 mol/L HNO3溶液,恰好使混合物溶解,同时收集到224 mL NO气体(标准状况)。下列说法不正确的是
| A.产物中硝酸铜的物质的量为0.025 mol |
| B.若混合物中Cu的物质的量为0.005 mol,则其中Cu2O、CuO的物质的量共0.020 mol |
| C.若混合物中含0.01 mol Cu,则其中Cu2O、CuO的物质的量均为0.005 mol |
| D.混合物中Cu的物质的量的取值范围为0.005 mol<n(Cu)<0.015 mol |
有4.8 g CuO、Fe2O3混合物跟足量CO充分反应后固体减少1.28 g,反应后全部气体用0.6 mol·L-1 Ba(OH)2溶液100 mL吸收。下列有关叙述中正确的是
| A.原混合物中CuO与Fe2O3物质的量的比为1∶2 |
| B.原混合物中CuO与Fe2O3的质量比为2∶1 |
| C.吸收CO2后溶液中一定有Ba(HCO3)2 |
| D.反应中生成的CO2体积为1.792 L |
对于实验Ⅰ~Ⅳ的实验现象预测正确的是
| A.实验Ⅰ:逐滴滴加盐酸时,试管中立即产生大量气泡 |
| B.实验Ⅱ:充分振荡后静置,下层溶液为橙红色,上层无色 |
| C.实验Ⅲ:从饱和食盐水中提取NaCl晶体 |
| D.装置Ⅳ:酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅直至褪去 |
有关纯碱和小苏打的叙述正确的是( )。
| A.等质量的Na2CO3、NaHCO3分别与足量稀盐酸反应,NaHCO3产生的CO2多 |
| B.等质量的Na2CO3、NaHCO3分别与足量的同种盐酸反应,NaHCO3消耗的盐酸多 |
| C.向NaHCO3溶液中滴入Ba(OH)2溶液无沉淀,而Na2CO3溶液中加入Ba(OH)2溶液出现白色沉淀 |
| D.Na2CO3和NaHCO3都既能与酸反应,又能与氢氧化钠反应 |