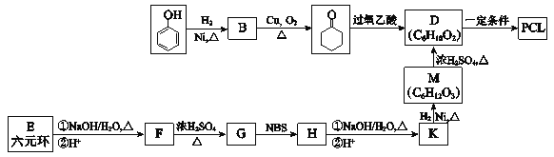
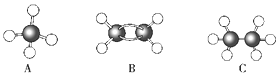
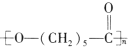��Ŀ����
����Ŀ���ȣ�Sr����þ��ͬ����Ԫ�أ��ȵĵ��ʼ��仯������;�㷺�������������������Ͻ𡢹��ܡ������ƣ�Sr��OH��2����ĥ��ʯ���ᴿ��Sr��NO3��2�����̻�װ�ã�SrCl2���������ݵȣ�
��1���ȣ�Sr��λ�����ڱ��ĵ����ڣ����壬�������ȣ�SrO2������Ԫ�صĻ��ϼ�Ϊ ��
��2���������ڳ����º�ˮ��Ӧ�����������ɣ�д���÷�Ӧ�Ļ�ѧ����ʽ
��3�������Ⱥܻ��ã��ڿ������ױ��������ɱ������У�����ţ���ˮ�ھƾ���ú��
��4���ȵ�����������ƣ���֪��CaCl2������ˮ��CaF2������ˮ����д�������Ⱥͷ����Ʒ�Ӧ�����ӷ���ʽ ��
��5�������������±���SrSO4��C�۵Ļ�����2molSrSO4��ȫ��Ӧ��ֻ��S����ԭ��ת��16mol���ӣ�ͬʱֻ����һ�ֿ�ȼ�����壮�÷�Ӧ�Ļ�ѧ����ʽ�� ��
��6����t��ʱ��ijSr��OH��2��ϡ��Һ��c��H+��=10��amolL��1 c��OH����=10��bmolL��1 �� ��֪a+b=12�������Һ����μ���pH=X�����ᣬ��û����Һ�IJ���pH�����ʾ��
��� | Sr��OH��2��Һ�����/mL | ��������/mL | ��Һ��pH |
�� | |||
�� | 22.00 | 18.00 | 7 |
�� | 22.00 | 22.00 | 6 |
��������Һ���ǰ�������仯����XΪ����������գ���
���𰸡�
��1���壻��A��+2
��2��Sr+2H2O=Sr��OH��2+H2��
��3����
��4��Sr2++2F��=SrF2��
��5��SrSO4+4C ![]() SrS+4CO��
SrS+4CO��
��6��4
���������⣺��1���ȣ�Sr����38��Ԫ�أ�������Ӳ㣬�����2�����ӣ�������λ�����ڱ��ĵ������ڣ��ڢ�A�壬�������ȣ�SrO2�������Ǹ�һ�ۣ�������Ԫ�صĻ��ϼ�Ϊ+2�ۣ����Դ��ǣ��壻��A��+2����2���������ڳ����º�ˮ��Ӧ���ǻ��õ�����ˮ�е������ӷ���������ԭ��Ӧ��������������Ӧ�Ļ�ѧ����ʽSr+2H2O=Sr��OH��2+H2�������Դ��ǣ�Sr+2H2O=Sr��OH��2+H2������3�������Ⱥܻ��ã�����ˮ�е��ⷢ���û���Ӧ�ʹ��ǻ����ⷢ���û���Ӧ�����Կɱ�����ú���У���ѡ���ۣ���4���ȵ�����������ƣ���֪��CaCl2������ˮ��CaF2������ˮ�����ϸ��ֽⷴӦ�������������Ⱥͷ����Ʒ�Ӧ�����ӷ���ʽΪ��Sr2++2F��=SrF2�������Դ��ǣ�Sr2++2F��=SrF2���� ��5����SrSO4��ֻ��S����ԭ����1mol SrSO4��Ӧ����ת��8mol����÷�Ӧ�Ļ�ѧ����ʽΪSrSO4+4C ![]() SrS+4CO�������Դ��ǣ�SrSO4+4C
SrS+4CO�������Դ��ǣ�SrSO4+4C ![]() SrS+4CO������6���ɢ�Sr��OH��2��Һ��pH=7��˵���������c��OH������22.00 mL��c��H+����18.00 mL=10��12+7����22.00+18.00��mL���ɢ۵�ǡ����ȫ�к�ʱ����Һ��pH=6��������������Ϊ22.00 mLʱ��ǡ����ȫ�кͣ�����c��H+����22.00 mL=c��OH������22.00 mL����֮������c��H+��=10��4mol/L��pH=4����X=4�����Դ��ǣ�4��
SrS+4CO������6���ɢ�Sr��OH��2��Һ��pH=7��˵���������c��OH������22.00 mL��c��H+����18.00 mL=10��12+7����22.00+18.00��mL���ɢ۵�ǡ����ȫ�к�ʱ����Һ��pH=6��������������Ϊ22.00 mLʱ��ǡ����ȫ�кͣ�����c��H+����22.00 mL=c��OH������22.00 mL����֮������c��H+��=10��4mol/L��pH=4����X=4�����Դ��ǣ�4��
�����㾫����������Ŀ����֪����������ͬһ������Ԫ�����ʵݱ������ԭ�ӽṹ�Ĺ�ϵ�����֪ʶ���Եõ�����Ĵ𰸣���Ҫ����ͬ����Ԫ�ص�ԭ�Ӱ뾶�����Ӱ뾶���ϵ����������磺O��S��Se��F����Cl����Br-��