题目内容
【题目】工业上常用氨气为原料制备硝酸,其中有一步非常重要的反应为:4NH3+5O2![]() 4NO+6H2O,该反应的氧化剂为________,还原剂为________;用单线桥法表示该氧化还原反应电子转移的方向和数目:________;若有标准状况下VL氨气完全反应,并转移n个电子,则阿伏加德罗常数(NA)可表示为________(写出含字母的表达式)。
4NO+6H2O,该反应的氧化剂为________,还原剂为________;用单线桥法表示该氧化还原反应电子转移的方向和数目:________;若有标准状况下VL氨气完全反应,并转移n个电子,则阿伏加德罗常数(NA)可表示为________(写出含字母的表达式)。
【答案】 O2 NH3 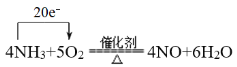
![]()
【解析】
反应4NH3+5O2![]() 4NO+6H2O中,N元素化合价由﹣3价升高到+2价,O元素化合价由0价降低到﹣2价,据此分析解答。
4NO+6H2O中,N元素化合价由﹣3价升高到+2价,O元素化合价由0价降低到﹣2价,据此分析解答。
反应4NH3+5O2![]() 4NO+6H2O中,N元素化合价由﹣3价升高到+2价,则NH3为还原剂,O元素化合价由0价降低到﹣2价,则O2为氧化剂,转移电子数为20e﹣,用单线桥法表示该氧化还原反应电子转移的方向和数目为:
4NO+6H2O中,N元素化合价由﹣3价升高到+2价,则NH3为还原剂,O元素化合价由0价降低到﹣2价,则O2为氧化剂,转移电子数为20e﹣,用单线桥法表示该氧化还原反应电子转移的方向和数目为: ;若有标准状况下V L氨气完全反应,并转移n个电子,则
;若有标准状况下V L氨气完全反应,并转移n个电子,则![]() ,所以阿伏加德罗常数(NA)可表示为
,所以阿伏加德罗常数(NA)可表示为![]() 。
。

【题目】草酸钴(CoOC2O3)用途广泛,一种利用水钴矿[主要成分为Co2O3,还含少量Fe2O3、Al2O3、MgO、MnO、CaO等]制取CoC2O4·2H2O的工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3的作用是将__________还原(填离子符号),该步反应的离子方程式为_________。
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+ ,氯元素被还原为最低价。该反应的离子方程式为_______________。
(3)加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是(用离子方程式表示,写出其中一个即可)_____________。
(4)萃取剂对金属离子的萃取率与pH的关系如右图所示。使用萃取剂适宜的pH=________(填序号)左右。

A.2.0 B.3.0 C.4.0
(5)滤液I“除钙,镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)=_____。