题目内容
重金属离子(Cu2+、Hg2+、Cd2+、Pb2+等)是常见的有毒污染物,水体、土壤及生物一旦受到重金属离子的污染就很难去除,重金属污染给生态环境和人类自身造成严重危害.某公司以含重金属的废水为原水,处理废水工艺流程如图1所示:

已知下列物质的Ksp:
请回答下列问题:
(1)OH-与S2-相比,除去废水中的Cu2+效果较好的是
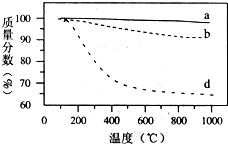
(2)图2为某些重金属离子在不同温度与pH下的平衡浓度:
从图中分析,除去废水中的重金属离子的最佳温度为

已知下列物质的Ksp:
| Cu(OH)2 | CuS | FeS | PbS | HgS | CdS |
| 2.2×10-20 | 8.5×10-45 | 6.3×10-18 | 3.4×10-28 | 4×10-53 | 8×10-29 |
(1)OH-与S2-相比,除去废水中的Cu2+效果较好的是
S2-
S2-
.(2)图2为某些重金属离子在不同温度与pH下的平衡浓度:
从图中分析,除去废水中的重金属离子的最佳温度为
60℃
60℃
,上述流程中NaOH的作用是调节溶液的PH为调节溶液的PH为8.8~9.0
调节溶液的PH为8.8~9.0
.分析:(1)由表中数据可知Ksp(CuS)<<Ksp[Cu(OH)2],所以CuS在水中溶解度比Cu(OH)2小;
(2)根据图中数据判断重金属离子的浓度最低时的温度;根据图中数据判断重金属离子的浓度最低时的PH,据此分析.
(2)根据图中数据判断重金属离子的浓度最低时的温度;根据图中数据判断重金属离子的浓度最低时的PH,据此分析.
解答:解:(1)由表中数据可知Ksp(CuS)<<Ksp[Cu(OH)2],所以CuS在水中溶解度比Cu(OH)2小,所以OH-与S2-相比,除去废水中的Cu2+效果较好的是S2-;
故答案为:S2-;
(2)由图中数据可知在60℃左右时重金属离子的浓度最低,所以除去废水中的重金属离子的最佳温度为:60℃;由图中数据可知PH在8.8~9.0时重金属离子浓度最低,所以NaOH的作用是调节溶液的PH为8.8~9.0;
故答案为:60℃;调节溶液的PH为8.8~9.0.
故答案为:S2-;
(2)由图中数据可知在60℃左右时重金属离子的浓度最低,所以除去废水中的重金属离子的最佳温度为:60℃;由图中数据可知PH在8.8~9.0时重金属离子浓度最低,所以NaOH的作用是调节溶液的PH为8.8~9.0;
故答案为:60℃;调节溶液的PH为8.8~9.0.
点评:本题考查了Ksp与溶解度的关系,根据图象判断沉淀形成的条件,充分利用图象中的信息,是解决问题的关键,题目难度中等.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
 为了开发新的功能材料,研究人员将碳纳米管a进行下列化学反应,在强氧化条件下,碳纳米管上的环被打开生成新的基团,得到改性碳纳米管.
为了开发新的功能材料,研究人员将碳纳米管a进行下列化学反应,在强氧化条件下,碳纳米管上的环被打开生成新的基团,得到改性碳纳米管.