题目内容
某溶液中可能含有Na+、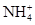 、Ba2+、
、Ba2+、
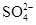 、I-、S2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是( )
、I-、S2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是( )
| A.Na+ | B.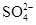 | C.Ba2+ | D.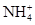 |
A
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列离子方程式书写正确的是
| A.Cu(OH)2中加入硫酸:OH- + H+ = H2O |
| B.Al2(SO4)3溶液中加入足量Ba(OH)2溶液:2Al3+ + 3SO42-+ 3Ba2+ + 6OH-= 2Al(OH)3↓ + 3BaSO4↓ |
| C.钠加入水中:Na+ 2H2O= Na+ + 2OH- + H2↑ |
D.向浓盐酸中加二氧化锰:MnO2+ 4H+ + 2Cl- Mn2+ + 2H2O + Cl2↑ Mn2+ + 2H2O + Cl2↑ |
在c(H+)/c(OH-)=10―12的水溶液中,能大量共存的离子组是
| A.Na+、K+、NO3-、CH3COO- | B.Fe3+、K+、SCN-、Cl- |
| C.K+、Al3+、Cl-、SO42- | D.Na+、Ba2+、I-、HCO3- |
下列各组离子一定能大量共存的是( )
| A.在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
| B.在强碱溶液中:Na+、K+、AlO2-、CO32- |
| C.在c(H+)=10—13 mol/L的溶液中:NH4+、Al3+、SO42-、NO3- |
| D.在pH=1的溶液中:K+、Fe2+、Cl—、NO3— |
下列分子或离子在指定的分散系中能大量共存的一组是
( )
| A.银氨溶液:Na+、K+、NO3—、NH3·H2O |
| B.空气:C2H2、CO2、SO2、NO |
| C.氢氧化铁胶体:H+、K+、S2-、Br- |
| D.高锰酸钾溶液:H+、Na+、SO42—、葡萄糖分子 |
类推是化学研究中常用的一种思维方式,下列有关离子反应方程式的类推正确的是( )。
| | 已知 | 类推 |
| A | 向次氯酸钙溶液中通CO2气体:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | 向次氯酸钙溶液中通SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| B | 用惰性电极电解硫酸铜溶液:2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ | 用铜电极电解硫酸铜溶液:2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
| C | 稀硫酸与Ba(OH)2溶液反应,pH=7时,2H++SO42—+Ba2++2OH-=BaSO4↓+2H2O | 硫酸氢钠溶液与Ba(OH)2溶液反应,pH=7时,2H++SO42—+Ba2++2OH-=BaSO4↓+2H2O |
| D | Ba(OH)2溶液逐滴滴入硫酸铝钾溶液至沉淀质量达到最大值:2Ba2++4OH-+Al3++2SO42—=2BaSO4↓+AlO2—+2H2O | Ba(OH)2溶液逐滴滴入硫酸铝铵溶液至沉淀质量达到最大值:2Ba2++4OH-+Al3++2SO42—=2BaSO4↓+AlO2—+2H2O |
在碱性条件下能够大量共存,而在强酸性条件下却能发生氧化还原反应的离子组是( )
A.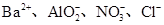 |
| B.K+、Na+、ClO-、Fe2+ |
C.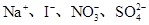 |
D.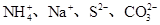 |
下列解释实验现象的反应方程式正确的是( )
| A.在CH3COONa溶液中,滴加酚酞溶液变红: CH3COO-+H2O  CH3COOH+OH- CH3COOH+OH- |
| B.在H2O2溶液中,滴加FeCl3溶液产生气泡: 2H2O2+2Cl-  2H2O+O2↑+Cl2↑ 2H2O+O2↑+Cl2↑ |
| C.将相互接触的铜片和锌片置于稀硫酸中,铜片表面有气泡产生: Cu+2H+  Cu2++H2↑ Cu2++H2↑ |
| D.向Cu(OH)2悬浊液中滴加Na2S溶液,蓝色沉淀变黑色: |
 CuS(s)+2OH-
CuS(s)+2OH- 下列离子方程式正确的是(双选) ( )。
| A.氯化铁溶液中加入铜粉:2Fe3++Cu===2Fe2++Cu2+ |
| B.向氢氧化亚铁中加入足量稀硝酸:Fe(OH)2+2H+===Fe2++2H2O |
| C.硫酸铜溶液与足量氢氧化钡溶液混合:Ba2++SO42—===BaSO4↓ |
| D.向硫酸氢钠溶液中滴加Ba(OH)2溶液至中性:2H++SO42—+Ba2++2OH-===BaSO4↓+2H2O |