题目内容
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如下图所示,则原混合液中Al3+、Mg2+、NH4+的物质的量分别是
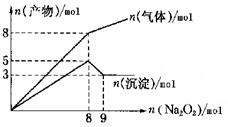
A.2mol、3mol、4mol B.2mol、3mol、8mol
C.3mol、2mol、8mol D.3mol、2mol、4mol
【答案】
A
【解析】
试题分析:将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合液中并微热,发生的反应有:
① 2Na2O2+2H2O=4NaOH+O2 ;② 3OH-+Al3+=Al(OH)3
;② 3OH-+Al3+=Al(OH)3 ;③Mg2++2OH-=Mg(OH)2
;③Mg2++2OH-=Mg(OH)2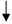 ;
;
④ NH4++OH-  NH3 +H2O
NH3 +H2O ;⑤ Al(OH)3+OH-=AlO2-+2H2O
。由反应⑤可得,生成的Al(OH)3为2mol,则Al3+的物质的量为2mol。
;⑤ Al(OH)3+OH-=AlO2-+2H2O
。由反应⑤可得,生成的Al(OH)3为2mol,则Al3+的物质的量为2mol。
考点:离子反应;化学计算
点评:此种题型要求掌握基本离子反应及化学计算

练习册系列答案
相关题目
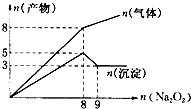 将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示,则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( )
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示,则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( )| A、2 mol、3 mol、8 mol | B、3 mol、2 mol、8 mol | C、2 mol、3 mol、4 mol | D、3 mol、2 mol、4 mol |
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如下图所示,则原混合液中Al3+、Mg2+、NH4+的物质的量分别是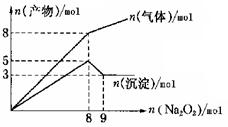
| A.2mol、3mol、4mol | B.2mol、3mol、8mol |
| C.3mol、2mol、8mol | D.3mol、2mol、4mol |
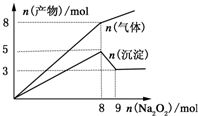 将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如下图所示.则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( )
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如下图所示.则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( ) (2013?防城港二模)某混合溶液中,可能大量含有的离子如下表:
(2013?防城港二模)某混合溶液中,可能大量含有的离子如下表: