��Ŀ����
����Ŀ����Ҫ�����
��1���뽫 Zn + 2Ag+ = 2Ag + Zn2+��Ƴ�˫Һԭ��أ�����������װ��ͼ����ע���缫�����Լ��������Һ___________

��2����д��ȩ-����ȼ�ϵ�أ��������ҺΪKOH���ĸ����缫��Ӧʽ___________________��
��3�����������һ�����͵�ȼ�ϵ�أ��������Һ��KOH��Һ����д�����������ĵ缫�ĵ缫��ӦʽΪ��________________________________________________________________��
��4������п�̸ɵ����һ��һ�ε�أ����Ϊ����п���м���̼��������Χ����̼�ۣ��������̣��Ȼ�п���Ȼ�淋���ɵ������õ���ڷŵ���̲���MnOOH���õ�ط�Ӧ�����ӷ���ʽΪ _________________________________________________________��
���𰸡� ��1��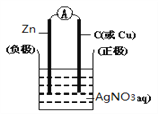 HCHO��4e����6OH��===CO
HCHO��4e����6OH��===CO![]() ��4H2O Al��3e����4OH��===AlO
��4H2O Al��3e����4OH��===AlO![]() ��2H2O Zn��2MnO2��2H����Zn2����2MnOOH��Zn��2MnO2��2NH4����Zn2����2MnOOH��2NH3
��2H2O Zn��2MnO2��2H����Zn2����2MnOOH��Zn��2MnO2��2NH4����Zn2����2MnOOH��2NH3
�������������������1������ Zn + 2Ag+ = 2Ag + Zn2+��Zn����������Ӧ������Zn��������Ag+������ԭ��Ӧ����Ag�����Կ��������������������Һ����ʯī����������2����ȩ-����ȼ�ϵ�أ���ȩ�ڸ���ʧ���ӣ���������������CO![]() ����3�����������ĵ缫�Ǹ����� ������أ����Ǹ��������ڼ���������ʧ��������AlO
����3�����������ĵ缫�Ǹ����� ������أ����Ǹ��������ڼ���������ʧ��������AlO![]() ����4���������⣬����п�̸ɵ�صĸ�����п��пʧ��������п���ӣ������Ƕ������̣��������̵õ�������MnOOH��
����4���������⣬����п�̸ɵ�صĸ�����п��пʧ��������п���ӣ������Ƕ������̣��������̵õ�������MnOOH��
��������1������ Zn + 2Ag+ = 2Ag + Zn2+��Zn����������Ӧ������Zn��������Ag+������ԭ��Ӧ����Ag�����Կ��������������������Һ����ʯī��������װ����ͼ ����2����ȩ-����ȼ�ϵ�أ���ȩ�ڸ���ʧ���ӣ���������������CO
����2����ȩ-����ȼ�ϵ�أ���ȩ�ڸ���ʧ���ӣ���������������CO![]() �������缫��Ӧʽ��HCHO��4e����6OH��===CO
�������缫��Ӧʽ��HCHO��4e����6OH��===CO![]() ��4H2O����3�����������ĵ缫�Ǹ�����������أ����ڼ���������ʧ��������AlO
��4H2O����3�����������ĵ缫�Ǹ�����������أ����ڼ���������ʧ��������AlO![]() ��������Ӧʽ��Al��3e����4OH��===AlO
��������Ӧʽ��Al��3e����4OH��===AlO![]() ��2H2O����4���������⣬����п�̸ɵ�صĸ�����п��пʧ��������п���ӣ������Ƕ������̣��������̵õ�������MnOOH�����Ըõ�ط�Ӧ�����ӷ���ʽΪZn��2MnO2��2H����Zn2����2MnOOH��
��2H2O����4���������⣬����п�̸ɵ�صĸ�����п��пʧ��������п���ӣ������Ƕ������̣��������̵õ�������MnOOH�����Ըõ�ط�Ӧ�����ӷ���ʽΪZn��2MnO2��2H����Zn2����2MnOOH��