题目内容
【题目】在10mL 0.05mo1/L的某金属硫酸盐溶液中,滴加0.1mo1/L BaCl2溶液,生成沉淀质量与加入BaCl2溶液体积关系如图所示,10mL该硫酸盐与足量的氢氧化钠完全反应生成10﹣3 mol沉淀,则该金属硫酸盐中金属元素的化合价为( ) 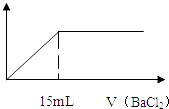
A.+1
B.+2
C.+3
D.+4
【答案】C
【解析】解:设该硫酸盐的化学式为R2(SO4)x , 则其化合价为+x价,10mL0.05mo1/L的该金属硫酸盐溶液物质的量为0.01L×0.05mo1/L=5×10﹣4mol,消耗的BaCl2溶液的物质的量为0.015L×0.1mo1/L=1.5×10﹣3mol,
R2(SO4)x +xBaCl2=xBaSO4↓+2RClx
1x
5×10﹣4mol 1.5×10﹣3mol
解得x=3,即金属元素的化合价为+3价;
故选C.

【题目】下图表示细胞内某些有机物的元素组成和功能关系,其中a、b代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,X、Y、Z、P分别为构成生物大分子的基本单位,请回答下列问题:

(1)图中A是__________________________。
(2)图中X是_____________________,Ⅰ在小麦种子中主要是指______________________。
(3)图中Z是____________,使用甲基绿、派洛宁混合染色剂染色,可使Ⅲ呈现__________色。
(4)图中P的结构通式为__________________,其形成Ⅳ的方式是_________;Ⅳ在结构上具有多样性,具体表现在______________________。
(5)用碘液、苏丹Ⅲ染液和双缩脲试剂测得甲、乙、丙三种植物的干种子中三大类有机物颜色反应如下表,其中“+”的数量代表颜色反应深浅程度,下列有关说法不正确的是 (____)
试剂种类 | 碘液 | 苏丹Ⅲ染液 | 双缩脲试剂 |
甲 | + + + + | + + | + |
乙 | + + | + + + + | + + |
丙 | + | + + | + + + + |
A.乙种子中主要含蛋白质
B.碘液、苏丹Ⅲ染液和双缩脲试剂与相应的物质发生的颜色反应分别是蓝色、橘黄色和紫色
C.在观察颜色时有可能用到光学显微镜
D.这三种试剂使用均不需要水浴加热

