题目内容
【题目】研究NO2、SO2 . CO等大气污染气体的处理具有重要意义.
(1)NO2可用水吸收,相应的化学反应方程式为
利用反应6NO2+8NH3 ![]() 7N2+12H2O也可处理NO2 . 当转移1.2mol电子时,消耗的NO2在标准状况下是 L.
7N2+12H2O也可处理NO2 . 当转移1.2mol电子时,消耗的NO2在标准状况下是 L.
(2)已知:2SO2(g)+O2(g)![]()
![]() 2SO3(g)△H=﹣196.6kJmol﹣1
2SO3(g)△H=﹣196.6kJmol﹣1
2NO(g)+O2(g)═2NO2(g)△H=﹣113.0kJmol﹣1
则反应SO2(g)+NO2(g)=SO3(g)+NO(g)的△H=kJmol﹣1
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
A.体系压强保持不变 B.混合气体颜色保持不变
C.SO2和NO的体积比保持不变 D.每消耗1molSO3的同时生成1mol NO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图所示.该反应△H0(填“>”或“<”)实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 . 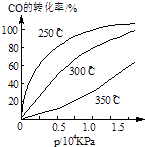
【答案】
(1)3NO2+H2O=2HNO3+NO;6.72
(2)﹣41.8;B;![]()
(3)<;在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失
【解析】解:(1)二氧化氮和水反应生成硝酸和一氧化氮,反应的化学方程式为:3NO2+H2O=2HNO3+NO,反应6NO2+8NH3![]() 7N2+12H2O中,6NO2中N元素化合价降低,由+4价降低到0价,则6molNO2参加反应,转移24mol电子,所以当转移1.2mol电子时,消耗NO20.3mol,体积为6.72L,所以答案是:3NO2+H2O=2HNO3+NO,6.72;(2)已知:①2SO2(g)+O2(g)2SO3(g)△H=﹣196.6kJmol﹣1②2NO(g)+O2(g)2NO2(g)△H=﹣113.0kJmol﹣1 , 利用盖斯定律将①×
7N2+12H2O中,6NO2中N元素化合价降低,由+4价降低到0价,则6molNO2参加反应,转移24mol电子,所以当转移1.2mol电子时,消耗NO20.3mol,体积为6.72L,所以答案是:3NO2+H2O=2HNO3+NO,6.72;(2)已知:①2SO2(g)+O2(g)2SO3(g)△H=﹣196.6kJmol﹣1②2NO(g)+O2(g)2NO2(g)△H=﹣113.0kJmol﹣1 , 利用盖斯定律将①× ![]() ﹣②×
﹣②× ![]() 得NO2(g)+SO2(g)SO3(g)+NO(g)△H=
得NO2(g)+SO2(g)SO3(g)+NO(g)△H= ![]() ×(﹣196.6kJmol﹣1)﹣
×(﹣196.6kJmol﹣1)﹣ ![]() ×(﹣113.0kJmol﹣1)=﹣41.8kJmol﹣1 , A.无论是否达到平衡,体系压强都保持不变,不能用于判断是否达到平衡状态,故A错误; B.混合气体颜色保持不变,说明浓度不变,达到平衡状态,故B正确; C.SO3和NO的计量数之比为1:1,无论是否达到平衡,二者的体积比保持不变,不能判断是否达到平衡状态,故C错误;
×(﹣113.0kJmol﹣1)=﹣41.8kJmol﹣1 , A.无论是否达到平衡,体系压强都保持不变,不能用于判断是否达到平衡状态,故A错误; B.混合气体颜色保持不变,说明浓度不变,达到平衡状态,故B正确; C.SO3和NO的计量数之比为1:1,无论是否达到平衡,二者的体积比保持不变,不能判断是否达到平衡状态,故C错误;
D.物质的量之比等于化学计量数之比,则每消耗1mol SO3的同时生成1molNO2 , 不能判断是否达到平衡状态,故D错误.
NO2(g)+SO2(g)SO3(g)+NO(g)
起始物质的体积 a 2a 0 0
转化物质的体积 x x x x
平衡物质的体积 a﹣x 2a﹣x x x
平衡时NO2与SO2体积比为1:6,即(1a﹣x):(2a﹣x)=1:6,故x= ![]() a,故平衡常数K=
a,故平衡常数K= ![]() =
= ![]() =
= ![]() =
= ![]() ,所以答案是:﹣41.8;B;
,所以答案是:﹣41.8;B; ![]() ;(3)由图可知,温度升高,CO的转化率降低,平衡向逆反应方向移动,故逆反应是吸热反应,正反应是放热反应,△H<0;压强大,有利于加快反应速率,有利于使平衡正向移动,但压强过大,需要的动力大,对设备的要求也高,故选择250℃、1.3×104kPa左右的条件.因为在250℃、压强为1.3×104 kPa时,CO的转化率已较大,再增大压强,CO的转化率变化不大,没有必要再增大压强.所以答案是:<,在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失.
;(3)由图可知,温度升高,CO的转化率降低,平衡向逆反应方向移动,故逆反应是吸热反应,正反应是放热反应,△H<0;压强大,有利于加快反应速率,有利于使平衡正向移动,但压强过大,需要的动力大,对设备的要求也高,故选择250℃、1.3×104kPa左右的条件.因为在250℃、压强为1.3×104 kPa时,CO的转化率已较大,再增大压强,CO的转化率变化不大,没有必要再增大压强.所以答案是:<,在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失.
【考点精析】解答此题的关键在于理解反应热和焓变的相关知识,掌握在化学反应中放出或吸收的热量,通常叫反应热,以及对化学平衡的计算的理解,了解反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.

 阅读快车系列答案
阅读快车系列答案【题目】除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是( )
选项 | 含杂质的物质 | 试剂 | 除杂方法 |
A | C2H4(SO2) | NaOH溶液 | 洗气 |
B | C6H6(苯酚) | 浓Br2水 | 过滤 |
C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
D | C2H2(H2S) | CuSO4溶液 | 洗气 |
A.A
B.B
C.C
D.D