题目内容
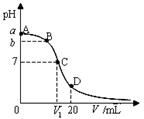
25℃,在20 mL 0.1mol/L 氨水溶液中逐滴加入0.2mol/L HCl溶液(如图),下列说法正确的是

- A.在A、C间任一点,溶液中一定都有:c(NH4+)>c(Cl—)>c(OH—)>c(H+)
- B.在C点,c<10,且有c(NH4+)=c(Cl—)=c(OH-)=c(H+)
- C.若25℃ 0.1mol/L 氨水电离度为1.33%,则b<a<12
- D.在D点:2c(NH4+)+2c(NH3·H2O)=c(Cl—)
CD
试题分析:根据图像可知,在A、C间任一点,溶液都显碱性,但氯离子浓度不一定大于c(OH—),A不正确;C点溶液显中性,根据电荷守恒可知,c(NH4+)=c(Cl—)>c(OH-)=c(H+),B不正确;25℃ 0.1mol/L 氨水电离度为1.33%,则氨水溶液中c(OH—)=1.33×10-3mol/L,则此氨水溶液的pH大于12,C正确;D溶液中的溶质是氯化铵和氯化氢,且二者的物质的量相等,所以根据物料守恒可知选项D正确,答案选CD。
考点:考查酸碱中和时溶液酸碱性的判断、离子浓度大小比较以及滴定曲线的判断
点评:该题是高考中的常见题型,属于综合性试题的考查,对学生的思维能力提出了较高的要求,本题贴近高考,综合性强,侧重对学生能力的培养,意在培养学生的逻辑推理能力和创新思维能力。该题的关键是在明确反应原理的基础上利用好几种守恒关系,即电荷守恒、物料守恒以及质子守恒,然后结合图像和题意灵活运用即可。
试题分析:根据图像可知,在A、C间任一点,溶液都显碱性,但氯离子浓度不一定大于c(OH—),A不正确;C点溶液显中性,根据电荷守恒可知,c(NH4+)=c(Cl—)>c(OH-)=c(H+),B不正确;25℃ 0.1mol/L 氨水电离度为1.33%,则氨水溶液中c(OH—)=1.33×10-3mol/L,则此氨水溶液的pH大于12,C正确;D溶液中的溶质是氯化铵和氯化氢,且二者的物质的量相等,所以根据物料守恒可知选项D正确,答案选CD。
考点:考查酸碱中和时溶液酸碱性的判断、离子浓度大小比较以及滴定曲线的判断
点评:该题是高考中的常见题型,属于综合性试题的考查,对学生的思维能力提出了较高的要求,本题贴近高考,综合性强,侧重对学生能力的培养,意在培养学生的逻辑推理能力和创新思维能力。该题的关键是在明确反应原理的基础上利用好几种守恒关系,即电荷守恒、物料守恒以及质子守恒,然后结合图像和题意灵活运用即可。

练习册系列答案
相关题目