题目内容
将2mol C气体在2 L的容器中混合并在一定条件下发生如下反应:2C(气) 2A(气)+B(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2A(气)+B(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.3 mol·L-1·s-1 ②用物质B表示的反应的平均速率为0.1 mol·L-1·s-1③2 s时物质C的转化率为40% ④2 s时物质B的浓度为0.2 mol·L-1
其中正确的是( )
 2A(气)+B(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2A(气)+B(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:①用物质A表示的反应平均速率为0.3 mol·L-1·s-1 ②用物质B表示的反应的平均速率为0.1 mol·L-1·s-1③2 s时物质C的转化率为40% ④2 s时物质B的浓度为0.2 mol·L-1
其中正确的是( )
| A.①③ | B.①④ | C.②③ | D.②③④ |
D
考查可逆反应的有关计算。经2 s(秒)后测得C的浓度为0.6 mol·L-1,则消耗C是2mol-0.6mol/L×2L=0.8mol,则
2C(气) 2A(气)+B(气)
2A(气)+B(气)
起始量(mol) 2 0 0
转化量(mol) 0.8 0.8 0.4
平衡量(mol) 1.2 0.8 0.4
所以用物质A表示的反应平均速率为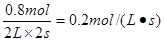
用物质B表示的反应的平均速率为
2 s时物质C的转化率为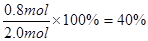
2s时物质B的浓度为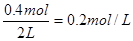
因此正确的答案是D。
2C(气)
 2A(气)+B(气)
2A(气)+B(气)起始量(mol) 2 0 0
转化量(mol) 0.8 0.8 0.4
平衡量(mol) 1.2 0.8 0.4
所以用物质A表示的反应平均速率为
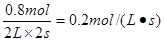
用物质B表示的反应的平均速率为

2 s时物质C的转化率为
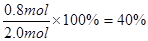
2s时物质B的浓度为
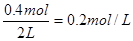
因此正确的答案是D。

练习册系列答案
相关题目
 nN(气)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,M的浓度为原来的80%,则
nN(气)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,M的浓度为原来的80%,则 CH3OH(g) ΔH=-90.7 kJ/mol):
CH3OH(g) ΔH=-90.7 kJ/mol): cC(s)+dD(g)达到平衡时,其反应的K值与温度有关。请写出该反应的平衡常数表达式
cC(s)+dD(g)达到平衡时,其反应的K值与温度有关。请写出该反应的平衡常数表达式  ,利用此概念可以讨论许多化学问题:
,利用此概念可以讨论许多化学问题: 4NO(g)+6H2O(g);假如温度保持不变并充入He,则平衡 (填“正向移动”、“逆向移动”、“不移动”),
4NO(g)+6H2O(g);假如温度保持不变并充入He,则平衡 (填“正向移动”、“逆向移动”、“不移动”), (混合气)将 (填写“变大”、“变小”或“不变”);
(混合气)将 (填写“变大”、“变小”或“不变”); C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是 
 2C(g)+D(g),下列物理量不能确定达到平衡状态的是
2C(g)+D(g),下列物理量不能确定达到平衡状态的是 2NH3,在一定温度下,向2L密闭容器中,加入2molN2和5molH2,一定条件下使之反应,经过2min后达到平衡状态并测得NH3为0.4mol,求:
2NH3,在一定温度下,向2L密闭容器中,加入2molN2和5molH2,一定条件下使之反应,经过2min后达到平衡状态并测得NH3为0.4mol,求: 2XY2
2XY2