题目内容
下列陈述I、II正确并且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | Fe2(SO4)3可以做净水剂 | Fe 3+水解成胶体可吸附水中的细小悬浮物 |
| B | 向Ba(NO3)2溶液中通入足量SO2,无明显现象 | 弱酸不能制强酸 |
| C | Cl2能使湿润的布条褪色 | Cl2具有漂白性 |
| D | 电解NaCl溶液制备金属钠 | NaCl是离子化合物 |
A
试题分析:硫酸铁是强酸弱碱盐,所含铁离子能水解,生成氢氧化铁胶体,氢氧化铁胶体具有很强的吸附性,可以将水中的细小悬浮物除去,因此硫酸铁可做净水剂,则陈述I、II均正确且有因果关系,故A正确;硝酸钡是硝酸盐,硝酸盐溶液具有氧化性,二氧化硫气体具有还原性,根据氧化还原反应中强制弱原理,向Ba(NO3)2溶液中通入足量SO2,生成硫酸钡沉淀、一氧化氮气体等,即Ba(NO3)2+ 3SO2+2H2O=BaSO4↓+2NO↑+2H2SO4,则陈述I、II均错,故B错;氯气与水发生氧化还原反应,生成盐酸和次氯酸,次氯酸具有强氧化性,具有漂白作者,能使布条褪色,虽然氯气也具有强氧化性,氮它没有漂白作用,则陈述I正确、II错,故C错;电解熔融氯化钠可以制备金属钠,因为氯化钠是离子化合物,电解氯化钠溶液不可能制备金属钠,因为溶液氢离子比钠离子容易得到电子,氢离子优先被还原为氢气,则陈述I错、陈述II正确,故D错。

练习册系列答案
相关题目

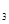 和2mol D
和2mol D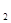 C
C