题目内容
汽车尾气净化中的一个反应如下:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-373.4kJ/mol
反应达到平衡后,改变某一个条件,下列示意图曲线①?⑧中正确的是( )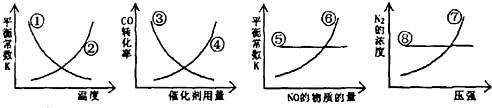
反应达到平衡后,改变某一个条件,下列示意图曲线①?⑧中正确的是( )

| A、①⑥⑧ | B、①⑤⑦ | C、②③④ | D、③⑥⑦ |
分析:平衡常数只受温度影响,升高温度平衡向吸热反应移动,该反应正反应为放热反应,故升高温度平衡向逆反应移动;
催化剂只改变化学反应速率,不改变化学平衡,物质转化率不变;
平衡常数只受温度影响,温度不变平衡常数不变,与物质的浓度无关;
压强增大,平衡正向进行,增大氮气的物质的量,氮气的浓度增大.
催化剂只改变化学反应速率,不改变化学平衡,物质转化率不变;
平衡常数只受温度影响,温度不变平衡常数不变,与物质的浓度无关;
压强增大,平衡正向进行,增大氮气的物质的量,氮气的浓度增大.
解答:解:平衡常数只受温度影响,升高温度平衡向吸热反应移动,该反应正反应为放热反应,故升高温度平衡向逆反应移动,平衡常数减小,故①正确②错误;
催化剂只改变化学反应速率,不改变化学平衡,物质转化率不变,故③④错误;
平衡常数只受温度影响,温度不变平衡常数不变,与物质的浓度无关,故⑤正确⑥错误;
压强增大,平衡正向进行,增大氮气的物质的量,氮气的浓度增大,⑦正确⑧错误;
综上所述①⑤⑦正确;
故选B.
催化剂只改变化学反应速率,不改变化学平衡,物质转化率不变,故③④错误;
平衡常数只受温度影响,温度不变平衡常数不变,与物质的浓度无关,故⑤正确⑥错误;
压强增大,平衡正向进行,增大氮气的物质的量,氮气的浓度增大,⑦正确⑧错误;
综上所述①⑤⑦正确;
故选B.
点评:本题考查影响平衡常数的因素、化学平衡的移动与图象等,难度不大,理解外界条件对平衡的影响是关键.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
 汽车尾气净化中的一个反应如下:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.8kJ?mol-1,在恒容的密闭容器中,反应达到平衡后,当改变其中一个条件X,Y随X的变化,符合图中曲线的是( )
汽车尾气净化中的一个反应如下:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.8kJ?mol-1,在恒容的密闭容器中,反应达到平衡后,当改变其中一个条件X,Y随X的变化,符合图中曲线的是( ) N2(g)+2CO2(g)
N2(g)+2CO2(g) N2(g) +2CO2(g)的△H=___________。
N2(g) +2CO2(g)的△H=___________。

