题目内容
己知:2C (s) + O2(g) = 2CO (g) △H = -221.0 kJ·mo1-1
2CO(g) + O2(g) = 2CO2 (g) △H = -566.0 kJ·mo1-1
2H2 (g) + O2 (g) = 2H2O (g) △H = -483.6 kJ·mo1-1
下列结论正确的是
A.H2的燃烧热△H=-241.8 kJ·mo1-1
B.炭和水蒸气转化为水煤气为放热反应
C.将24 g 炭完全转化为水煤气,再充分燃烧,整个过程反应热为-787.0 kJ·mo1-1
D.1molH2O(g)完全分解需要吸收241.8 kJ热量
CD

水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C (s) + H2O(g) ![]() CO (g) +H2 (g) △H = +131.3 kJ•mol-1
CO (g) +H2 (g) △H = +131.3 kJ•mol-1
(1)该反应的平衡常数K随温度的升高而___________(增大 / 减小 / 不变)。
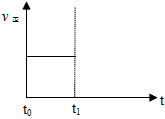
 (2)上述反应在t0时刻达到平衡(如下图),若在t1时刻改变某一条件,请在下图中继续画出t1时刻之后正反应速率(ν正)随时间的变化:
(2)上述反应在t0时刻达到平衡(如下图),若在t1时刻改变某一条件,请在下图中继续画出t1时刻之后正反应速率(ν正)随时间的变化:
① 缩小容器体积(用实线表示)
② 降低温度(用虚线表示)
(3)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
| 容器编号 | c(H2O)/mol·L-1 | c(CO)/mol·L-1 | c(H2)/mol·L-1 | ν正、ν逆比较 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | ________ | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ν正____ν逆 |
(4)己知:2C (s) + O2(g) = 2CO (g) △H = -221.0 kJ·mo1-1
2CO(g) + O2(g) = 2CO2 (g) △H = -566.0 kJ·mo1-1
2H2 (g) + O2 (g) = 2H2O (g) △H = -483.6 kJ·mo1-1
若将24g炭完全转化为水煤气,然后再充分燃烧,整个过程的焓变为△H = kJ/mol。
下列有关热化学方程式的叙述正确的是
| A.已知:正丁烷稳定性小于异丁烷,则CH3CH2CH2CH3(g)→(CH3)2CHCH3(g);△H>0 |
B.已知: OH-(ag)+H+(aq)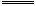 H2O(l);△H="-57.4" kJ/mol H2O(l);△H="-57.4" kJ/mol 则含20.0g NaOH的稀溶液与稀醋酸完全中和,放出28.7kJ的热量; |
C.已知:2H2O(l) 2H2(g)+O2(g);△H=" +483.6" kJ· mol—1,则氢气的燃烧热为241.8kJ/mol 2H2(g)+O2(g);△H=" +483.6" kJ· mol—1,则氢气的燃烧热为241.8kJ/mol |
| D.己知:2C(s)+2O2(g)=2CO2(g);△H12C(s)+O2(g)=2CO(g);△H2,则△H1>△H2 |
 H2O(l);△H=-57.4 kJ/mol
H2O(l);△H=-57.4 kJ/mol  2H2(g)+O2(g);△H= +483.6
kJ· mol—1,则氢气的燃烧热为241.8kJ/mol
2H2(g)+O2(g);△H= +483.6
kJ· mol—1,则氢气的燃烧热为241.8kJ/mol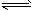 CO(g)+H2(g) △H= +131.3kJ·mol-1
CO(g)+H2(g) △H= +131.3kJ·mol-1