题目内容
某学习小组同学做了“海带成分中碘的检验”的实验。实验步骤如下: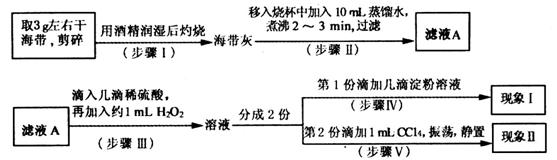
回答:
(1)灼烧海带所用到的仪器有:酒精灯、___________________。
(2)步骤Ⅱ中加热煮沸的目的是:_________________________________________________。
(3)步骤Ⅲ中发生反应的离子方程式为:________________;使用H2O2作为氧化剂的优点是:______________________________。
(4)现象Ⅰ为_____________________________;
现象Ⅱ为_____________________________。
(5)某同学提出:加有CCl4的溶液中应该加入NaOH溶液进行处理,然后再进行分液,他这样考虑的理由是:______________________________________________________________。
(1)坩埚、泥三角、三脚架;
(2)加速碘化物的溶解;
(3)2I-+2 H++H2O2====I2+2H2O 不产生污染物,不引入杂质
(4)溶液变蓝 下层呈紫红色 ;
(5)将易挥发的I2转化为无机盐,防止污染,同时可以回收CCl4

 名校课堂系列答案
名校课堂系列答案二氧化氮(NO2)是一种具有高度活性的气态物质,NO2与Na2O2均具有较强的氧化性,某研究性学习小组对二者能否发生反应进行探究。
【实验】
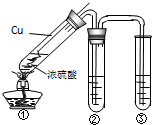
下列关于实验室制备NO2的说法正确的是_______
a.实验室常用铜和浓硝酸反应制取二氧化氮
b.二氧化氮常用向下排空气法收集
c.二氧化氮易溶于水,尾气可用水吸收.
d.用注射器收集的二氧化氮,压缩后颜色变浅
e.实验后容器中残留液需用碱液处理
【提出假设】
假设一:NO2与Na2O2二者不反应;
假设二:NO2能被Na2O2氧化;
假设三:
【查阅文献】
NO2在反应中能生成HNO3和HNO2;HNO2旣有氧化性,又有还原性,能被强氧化剂如KMnO4氧化。
【设计实验】
(1)实验时,将NO2气体通入盛有Na2O2的玻璃管中,淡黄色粉末完全变成白色,说明假设 不成立。
(2)若假设二成立,反应的化学方程式是 。
(3)为验证假设二是否成立,该小组同学做了如下定性实验研究,请完成下表内容。
|
实验步骤 (不要求写具体操作过程,仪器任选) |
预期的实验现象及结论 |
|
取适量的白色固体置于试管中,………… |
|
【定量分析】
若实验前该小组同学用托盘天平称量过氧化钠的质量为3.9g,充分反应后白色固体质量为8.4g,该小组同学得出假设2不成立的结论。你是否同意他们的结论,并简述理由:

 化学是一门以实验为基础的自然科学.
化学是一门以实验为基础的自然科学.