题目内容
8.在2SO2(g)+O2(g)?2SO3(g)的反应中,工业生产上为了充分利用SO2所采用的方法是( )| A. | 增加O2的浓度 | B. | 增加SO2的浓度 | C. | 使用催化剂 | D. | 增加SO3的量 |
分析 工业生产上为了充分利用SO2即要提高二氧化硫的转化率,据此分析.
解答 解:A.增加O2的浓度,应反应没有停止,提高二氧化硫的转化率,故A正确;
B.增加SO2的浓度,二氧化硫的转化率降低,故B错误;
C.加入催化剂,二氧化硫的转化率不变,故C错误;
D.增加SO3的量,平衡逆向移动,二氧化硫的转化率降低,故D错误.
故选A.
点评 本题考查化学反应平衡的移动原理,为高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
16.钾和钠化学性质相似,能最好地解释这个事实的是( )
| A. | 它们的最外层电子数相同 | B. | 它们的原子半径相差不大 | ||
| C. | 它们都是金属元素 | D. | 它们的最高化合价相同 |
3.关于能源,以下说法中不正确的是( )
| A. | 煤、石油、天然气等燃料属不可再生能源 | |
| B. | 煤、石油、水煤气可从自然界直接获取,属一级能源 | |
| C. | 太阳能是一级能源、新能源、可再生能源 | |
| D. | 潮汐能来源于月球引力做功 |
13.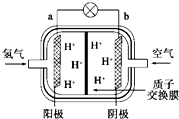 为体现“绿色奥运”、“科技奥运”的理念,中国将在2008年北京奥运会时推出国产燃料电池汽车,作为马拉松领跑车和拍摄车,该车装有“绿色心脏”--质子交换膜燃料电池.下图是某科技杂志登载的该电池原理示意图.下列叙述正确的是( )
为体现“绿色奥运”、“科技奥运”的理念,中国将在2008年北京奥运会时推出国产燃料电池汽车,作为马拉松领跑车和拍摄车,该车装有“绿色心脏”--质子交换膜燃料电池.下图是某科技杂志登载的该电池原理示意图.下列叙述正确的是( )
 为体现“绿色奥运”、“科技奥运”的理念,中国将在2008年北京奥运会时推出国产燃料电池汽车,作为马拉松领跑车和拍摄车,该车装有“绿色心脏”--质子交换膜燃料电池.下图是某科技杂志登载的该电池原理示意图.下列叙述正确的是( )
为体现“绿色奥运”、“科技奥运”的理念,中国将在2008年北京奥运会时推出国产燃料电池汽车,作为马拉松领跑车和拍摄车,该车装有“绿色心脏”--质子交换膜燃料电池.下图是某科技杂志登载的该电池原理示意图.下列叙述正确的是( )| A. | 工作时,“阳极”周围溶液的酸性增强 | |
| B. | 氢气在电极上发生还原反应 | |
| C. | 图中标出的“阴极”实际是原电池的负极 | |
| D. | 工作过程中,质子(H+)从“阴极”一边透过质子交换膜移动到“阳极”一边与OH-反应生成水 |
20.在下列转化中必须加入还原剂才能实现的是( )
| A. | CaCO3→CO2 | B. | CuSO4→Cu | C. | H2O→H2 | D. | C→CO2 |
18.工业上冶炼金属,常用的方法有四种:Ⅰ、热分解法,Ⅱ、热还原法,Ⅲ、电解法,Ⅳ、湿法冶金.下表中金属与常用冶炼方法相符的是( )
| 金属 | 冶炼方法 | |
| A | 钾、钙 | Ⅳ |
| B | 钠、铝 | Ⅲ |
| C | 铜、铁 | Ⅰ |
| D | 银、汞 | Ⅱ |
| A. | A | B. | B | C. | C | D. | D |
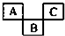 如图是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等.
如图是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等.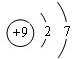 ;B的最高价氧化物对应的水化物的化学式为H2SO4.
;B的最高价氧化物对应的水化物的化学式为H2SO4.