题目内容
(10分)普通玻璃是 (混合物、纯净物)玻璃可在一定温度范围内软化,制成工艺品等。这是因为玻璃是一种 物质,没有固定的 。 盛强碱溶液的磨口试剂瓶都不能用玻璃瓶塞的原因是
。
变色眼镜的玻璃片中含有少量的溴化银和微量氧化铜。当玻璃受到阳光照射时,因为发生 反应(用化学方程式表示),而使玻璃由无色变为暗棕色。
。
变色眼镜的玻璃片中含有少量的溴化银和微量氧化铜。当玻璃受到阳光照射时,因为发生 反应(用化学方程式表示),而使玻璃由无色变为暗棕色。
(10分)
混合物 玻璃态 熔点 2OH-+SiO2 =SiO32-+H2O 2AgBr = Ag+Br2
混合物 玻璃态 熔点 2OH-+SiO2 =SiO32-+H2O 2AgBr = Ag+Br2
试题分析:普通玻璃的主要成分是硅酸钠、硅酸钙和二氧化硅,是混合物,玻璃可在一定温度范围内软化,制成工艺品等。这是因为玻璃是一种玻璃态物质,没有固定的熔点。玻璃中的二氧化硅能和氢氧化钠溶液反应蔬菜粘性强的硅酸钠,是瓶口和玻璃塞粘合在一起而不易打开,因此应该有橡胶塞,不能用玻璃塞。溴化银见光易分解蔬菜银和单质溴,从而可以制成有色眼镜。
点评:本题是基础性试题的考查,主要是检验学生对有关玻璃基础知识的熟悉掌握程度,侧重对学生基础知识的巩固与训练,有助于培养学生的学习兴趣和学习积极性。

练习册系列答案
相关题目
 CH3OH(g)△H1=-116 kJ·mol-1
CH3OH(g)△H1=-116 kJ·mol-1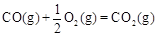 △H2=-283 kJ·mol-1
△H2=-283 kJ·mol-1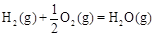 △H3=-242 kJ·mol-1
△H3=-242 kJ·mol-1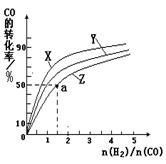
 CH3OH(g)的平衡常数K= 。
CH3OH(g)的平衡常数K= 。  CaSiO3+CO↑
CaSiO3+CO↑