题目内容
某研究小组模拟工业上以黄铁矿为原料制备硫酸的第一步反应如下:
4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
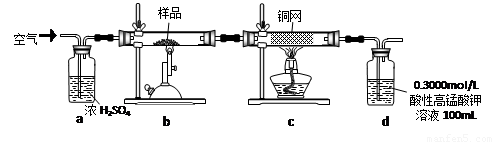
进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。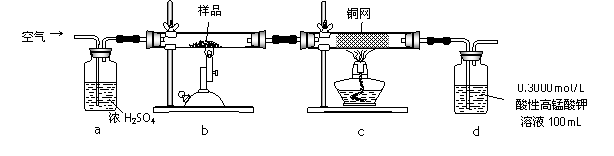
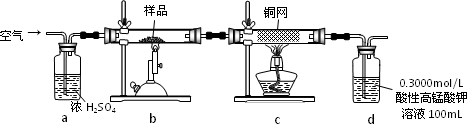
实验步骤:称取研细的样品4.000g放入上图b装置中,然后在空气中进行煅烧。为测定未反应高锰酸钾的量(假设其溶液体积保持不变),实验完成后取出d中溶液10mL置于锥形瓶里,用0.1000mol/L草酸(H2C2O4)标准溶液进行滴定。
(已知:5SO2 + 2KMnO4 + 2H2O == K2SO4 + 2MnSO4 + 2H2SO4 )
请回答下列问题:
(1)称量样品质量能否用托盘天平_______(填“能”或“不能”),取出d中溶液10mL需要用______准确量取(填序号)
A.容量瓶 B.量筒 C.碱式滴定管 D.酸式滴定管
 (2)上述反应结束后,仍需通一段时间的空气,其目的是_______________________________
(2)上述反应结束后,仍需通一段时间的空气,其目的是_______________________________
(3)已知草酸与高锰酸钾酸性溶液作用有CO2和Mn2+等物质生成,则滴定时发生反应的离子方程式为_______________________________________﹔判断滴定到达终点的方法是_____________________________________________
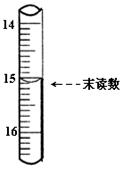
(4)已知滴定管初读数为0.10mL,末读数如右图所示,消耗草酸溶液的体积为___________mL,
下列操作会导致该样品中FeS2的纯度测定结果偏高的是_________(填序号)
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(5)该样品中FeS2的纯度为__________________
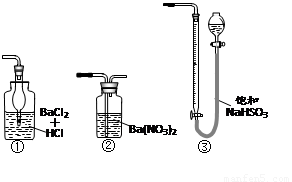
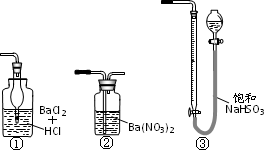
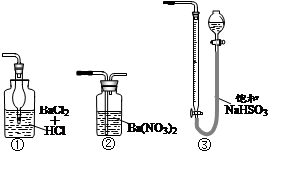
(6)若用下图装置替代上述实验装置d,同样可以达到实验目的的是_______(填编号)
 |
(1)不能 , D(每空1分)
(2)促进装置中的二氧化硫气体全部吸收 (2分,意思对即可给分)
(3)2MnO4—+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O (3分,没配平0分,气体符号不写不扣分,写化学方程式不给分), 滴入最后一滴草酸溶液, 溶液由紫红色变为无色,且半分钟内不恢复(4分)
(4) 15.00(1分) , C (1分)
(5) 90% (2分,写成0.9或90.00%也可以,有效数字不考虑)
(6) ② (1分,多选不给分)

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案



 2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。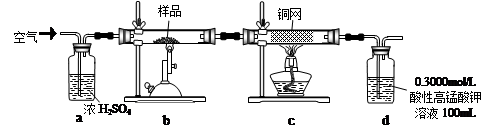

 2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。