题目内容
在28.5gRCl2(R为某金属)固体中,含有0.6molCl-,则RCl2的摩尔质量为________,R的原子量为________;如溶于水配成500mL溶液,则该物质的物质的量浓度为________.
95g/mol 24 0.6mol/L
分析:根据分子式与氯离子间的关系计算RCl2的物质的量,再根据物质的量、质量、摩尔质量之间的关系式计算其摩尔质量;根据分子量与原子量的关系计算其原子量;根据物质的量浓度、物质的量、溶液体积之间的关系式计算其物质的量浓度.
解答:①RCl2 →2Cl-,
1 2
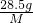 0.6mol
0.6mol
M=95g/mol
②分子量在数值上等于其摩尔质量,所以其分子量为95,所以R的原子量为95-35.5×2=24
③RCl2 →2Cl-,
1 2
0.3mol 0.6mol
C= =0.6mol/L
=0.6mol/L
点评:本题考查的是物质的量浓度的有关计算,侧重考查学生对各物理量关系的掌握程度.
分析:根据分子式与氯离子间的关系计算RCl2的物质的量,再根据物质的量、质量、摩尔质量之间的关系式计算其摩尔质量;根据分子量与原子量的关系计算其原子量;根据物质的量浓度、物质的量、溶液体积之间的关系式计算其物质的量浓度.
解答:①RCl2 →2Cl-,
1 2
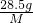 0.6mol
0.6molM=95g/mol
②分子量在数值上等于其摩尔质量,所以其分子量为95,所以R的原子量为95-35.5×2=24
③RCl2 →2Cl-,
1 2
0.3mol 0.6mol
C=
 =0.6mol/L
=0.6mol/L点评:本题考查的是物质的量浓度的有关计算,侧重考查学生对各物理量关系的掌握程度.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目