题目内容
用于“点豆腐”的氯化镁结晶水合物化学式是MgCl2?nH2O,取10.15g此结晶水合物溶于水,加入足量的AgNO3溶液,得到氯化银沉淀14.35g.则n的值是( )A.2
B.4
C.6
D.8
【答案】分析:MgCl2?nH2O此结晶水合物溶于水,加入足量的AgNO3溶液,硝酸银会和氯化镁之间发生反应生成产点氯化银,根据氯化银的质量确定结晶水合物的物质的量,进而根据质量确定水合物的相对分子质量以及n的值.
解答:根据氯元素周守,则解:MgCl2?nH2O-2AgCl↓
95+18n 287
10.15g 14.35g
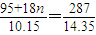
解得n=6.
故选C.
点评:本题考查学生物质分子式的确定方面的知识,注意原子守恒的思想在解题中的灵活应用是解题的关键,难度不大.
解答:根据氯元素周守,则解:MgCl2?nH2O-2AgCl↓
95+18n 287
10.15g 14.35g
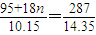
解得n=6.
故选C.
点评:本题考查学生物质分子式的确定方面的知识,注意原子守恒的思想在解题中的灵活应用是解题的关键,难度不大.

练习册系列答案
相关题目
下列事实:①用盐卤点豆腐 ②用明矾净水 ③河海交汇处可沉积沙洲 ④钢笔使用两种不同颜色的墨水,易出现堵塞⑤FeCl3溶液用于伤口止血.其中与胶体知识有关的是( )
| A、①②③ | B、③④ | C、①③⑤ | D、全部都是 |