题目内容
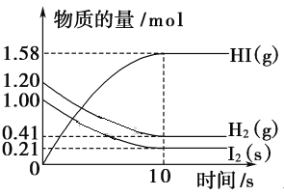
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示。
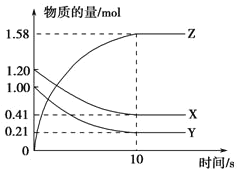
(1)从反应开始到10 s,用Z表示的反应速率为____。X的物质的量浓度减少了___,Y的转化率为_____。
(2)该反应的化学方程式为____。
(3)10s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示。则下列说法符合该图像的是_____。
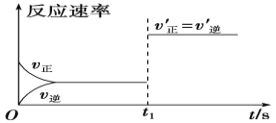
A.t1时刻,增大了X的浓度 B.t1时刻,缩小了容器体积
C.t1时刻,升高了体系温度 D.t1时刻,使用了催化剂
【答案】0.079mol/(L·s) 0.395mol/L 79% X(g)+Y(g)![]() 2Z(g) BD
2Z(g) BD
【解析】
由图可知,X、Y为反应物,Z为生成物,X、Y、Z的化学计量数之比为(1.20—0.41)mol:(1.00—0.21)mol:(1.58—0)mol=1:1:2,则反应的化学方程式为X(g)+Y(g)![]() 2Z(g),该反应是一个气体体积不变反应。
2Z(g),该反应是一个气体体积不变反应。
(1)由图像可知,从反应开始到10 s,反应生成Z的物质的量为1.58mol,2L容器中Z浓度增加的量为![]() =0.79mol/L,则用Z表示的反应速率为
=0.79mol/L,则用Z表示的反应速率为![]() =
=![]() =0.079mol/(L·s);X的物质的量减少了(1.20—0.41)mol=0.79mol,2L容器中X的物质的量减少了
=0.079mol/(L·s);X的物质的量减少了(1.20—0.41)mol=0.79mol,2L容器中X的物质的量减少了![]() =0.395mol/L;Y的起始物质的量为1.00mol,反应消耗Y的物质的量为(1.00—0.21)mol=0.79mol,则Y的转化率为
=0.395mol/L;Y的起始物质的量为1.00mol,反应消耗Y的物质的量为(1.00—0.21)mol=0.79mol,则Y的转化率为![]() ×100%=79%,故答案为:0.079mol/(L·s);0.395mol/L;79%;
×100%=79%,故答案为:0.079mol/(L·s);0.395mol/L;79%;
(2)反应中各物质的物质的量变化量之比等于各物质的化学计量数之比,由图可知,X、Y为反应物,Z为生成物,X、Y、Z的化学计量数之比为(1.20—0.41)mol:(1.00—0.21)mol:(1.58—0)mol=1:1:2,则反应的化学方程式为X(g)+Y(g)![]() 2Z(g),故答案为:X(g)+Y(g)
2Z(g),故答案为:X(g)+Y(g)![]() 2Z(g);
2Z(g);
(3)由反应方程式可知,该反应是一个气体体积不变反应,由图可知,改变反应条件,反应速率加快,但是正逆反应速率相等,化学平衡不移动,则改变的条件可能为缩小容器的容积增大压强或加入合适的催化剂,BD正确,故答案为:BD。

 阅读快车系列答案
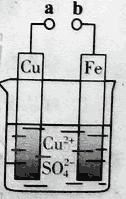
阅读快车系列答案【题目】某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
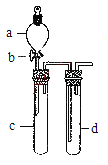
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是_____________________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是____________________。再由a向c中加2 mL蒸馏水,c中的实验现象是 ___________________________。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是_____________。理由是_____________。
方案 | 反应物 |
甲 | Cu、浓HNO3 |
乙 | Cu、稀HNO3 |
丙 | Cu、O2、稀HNO3 |