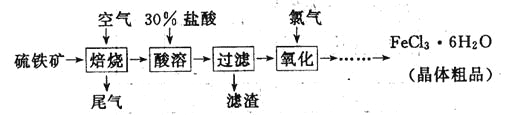
题目内容
【题目】把铝、铁混合物 1.1g 溶于200mL 5molL ﹣1盐酸中,反应后盐酸的浓度变为4.6molL ﹣1(溶液体积变化忽略不计).求:
(1)反应中消耗HCl的物质的量.
(2)该混合物中铝、铁的物质的量.
【答案】
(1)解:消耗HCl的物质的量为0.2L×5molL﹣1﹣0.2L×4.6molL﹣1=0.08mol,
答:反应中消耗HCl的物质的量为0.08mol;
(2)解:设Al、Fe的物质的量分别为x、y
由2Al+6HCl═2AlCl3+3H2↑、Fe+2HCl═FeCl2+H2↑
则
Al | ~ | 3HCl |
x | 3x |
Fe | ~ | 2HCl |
y | 2y |
![]() ,
,
解得x=0.02mol、y=0.01mol,
答:该混合物中铝、铁的物质的量分别为0.02mol、0.01mol.
【解析】(1)利用n=cV,根据反应前HCl的物质的量减去反应后溶液中HCl的物质的量来计算;(2)根据金属的质量之和为1.1g及反应中消耗的HCl来列式计算即可.

【题目】某化学小组以苯甲酸为原料,制取苯甲酸甲酯.已知有关物质的沸点如下表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
沸点/℃ | 64.7 | 249 | 199.6 |
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入9.6ml(密度约为1.27g.ml-1)苯甲酸和20mL甲醇(密度约0.79g·mL﹣1),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1) 加入碎瓷片的作用是 ;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作时 (填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(2)浓硫酸的作用是 混合液体时最后加入浓硫酸的理由: 。
(3)甲、乙、丙三位同学分别设计了如图三套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点最好采用装置 (填“甲”或“乙”或“丙”)。

Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中含有少量甲醇、硫酸、苯甲酸和水,现拟用下列流程进行精制,请根据流程图写出操作方法的名称,操作Ⅱ 。

(5)不能用NaOH溶液代替饱和碳酸钠溶液的原因是 。
(6)列式计算,苯甲酸甲酯的产率是 。