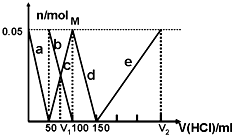
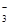题目内容
溶液X中可能含有K+、Mg2+、Al3+、AlO、SiO、CO、SO、SO中的若干种离子。某同学对该溶液进行了如下实验:
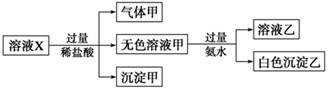
下列判断正确的是

下列判断正确的是
| A.气体甲一定是纯净物 |
| B.沉淀乙为Mg(OH)2 |
| C.沉淀甲是硅酸和硅酸镁的混合物 |
D.溶液X中一定存在K+、AlO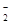 和SiO 和SiO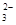 离子 离子 |
D
试题分析:加HCl有气体说明有CO32-或SO32-,或两者都有,生成的气体是二氧化碳或二氧化硫,或两者都有,一定不存在和碳酸根或亚硫酸根离子不共存的离子,所以不存在镁离子、铝离子;加盐酸有沉淀,说明一定有硅酸根离子,硅酸是沉淀;加入过量氨水(提供OH-)有沉淀生成,只能是氢氧化铝沉淀,说明此时溶液中存在铝离子,但是原来溶液中的铝离子一定不能存在,所以该铝离子是偏铝酸根离子和盐酸反应生成的,所以,一定存在偏铝酸根离子,要保证溶液电中性,只有K+这一个阳离子,所以一定存在钾离子。A、加HCl有气体说明有CO32-或SO32-,生成的气体是二氧化碳或二氧化硫或两者的混合气体,故A错误;B、沉淀乙为氢氧化铝,B不正确;C、溶液中一定含有CO32-或SO32-,或两者都有,则一定不含有镁离子,它们和镁离子都不共存,所以沉淀甲是硅酸,不可能是硅酸镁,故C错误;D、原来溶液中K+、AlO
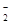 和SiO
和SiO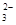 离子一定存在,故D正确,故选D。
离子一定存在,故D正确,故选D。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
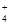 、I-、NO
、I-、NO