��Ŀ����
��֪��������������У���ͨ�������Li2O�����������Na2O2�����������KO2�����������RbO3�����к����߾�����H2O��CO2��Ӧ����O2 ��
��1�����ҵ��Ϊ���ܱ��ַɴ������ڿ����ɷֵ��ȶ������ѧ�ҽ����˴�����̽�����еĿ�ѧ������ˡ������������ﴦ��ϵͳ���������ϰ������ڵĿ���ͨ��ʢ�н�����������Թ�������Ϊ���������������Ѵ����������������ա�ÿ���Աƽ��ÿ����Ҫ����0.9 kg����������1.0 kg������̼���йط�Ӧ�Ļ�ѧ����ʽΪ �� ����������������������ʱ��Ϊ���ܱ��ַɴ������ڿ����ɷֵ��ȶ�����Ӧ��ȡ�Ĵ�ʩ��___________________________________��
��2��������O2�����ӶԽ����к���ʹ�˹���˥�ϣ����ڴ���SOD�����¿ɷ������·�Ӧ������ɸ÷�Ӧ�����ӷ���ʽ�� O2�� + H2O �� H2O2�� O2��
��3��Na2O2��K2O2��CaO2�Լ�BaO2���������������ɹ������⣬Ŀǰʵ������ȡ���������ͨ������ij�ֹ�������������ϡ�������ã����˼����Ƶá����ʺϵĹ��������� ��д����ʽ��
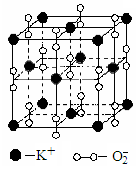
��4�������£��������ؾ����������ṹ�����������Ļ��ϼ۲���Ϊ0�ۣ�����Ϊ��2�ۡ���ͼΪ�������ؾ����һ����������������С���ظ���Ԫ������ÿ���������ؾ������� ��K���� ��O2�����þ����У�0����ԭ���룭2����ԭ�ӵ���Ŀ��Ϊ
��1����ÿ��1�֣�2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2H2O=4NaOH+O2������������ˮ������
��2����2�֣� 2 O2�� + 2 H2O �� 1 H2O2��1 O2�� 2 OH��
��3����1�֣�BaO2�ĵ���ʽ
��4����1��+1��+2�֣�4��4 3��1
����:

 ��У����ϵ�д�
��У����ϵ�д�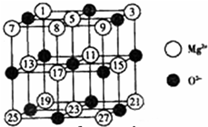 ��2008?�㶫��þ��ͭ�Ƚ��������������ڶ���ø�ĸ����ӣ���ҵ�ϴӺ�ˮ����ȡþʱ�����Ʊ���ˮ�Ȼ�þ��Ȼ�������ڵ�⣬�õ�����þ��
��2008?�㶫��þ��ͭ�Ƚ��������������ڶ���ø�ĸ����ӣ���ҵ�ϴӺ�ˮ����ȡþʱ�����Ʊ���ˮ�Ȼ�þ��Ȼ�������ڵ�⣬�õ�����þ�� ��Cu��I����I��ʾ���ϼ�Ϊ+1��ʱ���ֱ��γ�a��b��
��Cu��I����I��ʾ���ϼ�Ϊ+1��ʱ���ֱ��γ�a��b��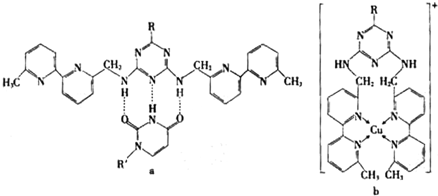
 O2���������������ɹ������⣬Ŀǰʵ������ȡ���������ͨ������ij�ֹ�������������ϡ�������ã����˼����Ƶá����ʺϵĹ��������� ��д����ʽ��
O2���������������ɹ������⣬Ŀǰʵ������ȡ���������ͨ������ij�ֹ�������������ϡ�������ã����˼����Ƶá����ʺϵĹ��������� ��д����ʽ�� ��������ṹ�����������Ļ��ϼ۲���Ϊ0�ۣ�����Ϊ��2�ۡ���ͼΪ�������ؾ����һ����������������С���ظ���Ԫ������ÿ���������ؾ������� ��K���� ��O2�����þ����У�0����ԭ���룭2����ԭ�ӵ���Ŀ��Ϊ
��������ṹ�����������Ļ��ϼ۲���Ϊ0�ۣ�����Ϊ��2�ۡ���ͼΪ�������ؾ����һ����������������С���ظ���Ԫ������ÿ���������ؾ������� ��K���� ��O2�����þ����У�0����ԭ���룭2����ԭ�ӵ���Ŀ��Ϊ