��Ŀ����
(1)(2)���ʯ��ʯī��Ϊ___________����֤����ʵ��______________________�����ʯ��ʯī�������ʲ�ͬ��ԭ���� _________________________________��
(3)�õ绡��ʹʯī��������ý϶�IJ�������״�ṹ����Է�������Ϊ720��840�����ַ��ӣ����������ʵķ���ʽ��___________��___________�����Ǻͽ��ʯ�����ϵ��___________����Է�������Ϊ720�ķ��ӿ���������γ�һ�ֳ����������������Է�������Ϊ837����˳�������(��ѧʽ)Ϊ___________��
����:����Ŀ������ͬλ�ء�ͬ���������ʶ�����жϡ�Ԫ�ذ�������ͬλ�ص�ԭ�ӡ����ӡ����ӵ����ӣ�ͬ��Ԫ����ɵ����ʲ�ͬ�ĵ��ʻ���ͬ�������壬ͬ��������֮����һ����������Ҳ�ɻ���ת�������Ǻ��������ʷ�Ӧʱ���������ͬ�ģ�������ṹ��ͬ���������ʲ�ͬ��
���������������ʵ���Է�����������������ַ��ӵĻ�ѧʽ�ֱ�ΪC60��C70���������ϻ�ѧʽ��Kԭ��������ã�![]() =3�����Է���ʽΪK3C60��
=3�����Է���ʽΪK3C60��
��:(1)��Ԫ�ص����ֲ�ͬ����(��뭡�뮡��ԭ�ӣ������ӣ������) ��Ԫ�� ����ͬλ��ԭ��
(2)ͬ�������� ���ֵ����ڴ�������ȼ�ղ��ﶼ��CO2 ������ԭ�����з�ʽ��ͬ
(3)C60 C70 ͬ�������� K3C60

��10�֣�Ϊ�˺������û�ѧ�ܣ�ȷ����ȫ���������������Ҫ��ֿ��ǻ�ѧ��Ӧ�ķ�Ӧ�ȣ�����ȡ��Ӧ��ʩ����ѧ��Ӧ�ķ�Ӧ��ͨ����ʵ����вⶨ��Ҳ�ɽ����������㡣
��1���������������Ȼ�ѧ����ʽ��?��a b����>,= , <��
H2(g)+O2(g) �� H2O(g)����H1��a kJ��mol-1?
H2(g)+O2(g) �� H2O(l) ��H2��b kJ��mol-1??
��2������̬��̬ԭ���γ�1mol��ѧ���ͷŵ���������м��ܡ��ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̡��ڻ�ѧ��Ӧ�����У���ѧ����Ҫ�����������γɻ�ѧ���ֻ��ͷ�������
| ��ѧ�� | H��H | N��H | N��N |
| ����/kJ��mol��1 | 436 | 391 | 945 |
��֪��ӦN2(g)��3H2(g)2NH3(g) ��H��a kJ��mol��1���Ը��ݱ������м������ݹ���a ��ֵ��_______________��
��3�����ݸ�˹���ɿ��Զ�ijЩ����ͨ��ʵ��ֱ�Ӳⶨ�Ļ�ѧ��Ӧ�ķ�Ӧ�Ƚ������㡣
��֪��C(s)��O2(g)��CO2(g) ��H1����393.5kJ��mol��1
2H2(g)��O2(g)��2H2O(l) ��H2����571.6kJ��mol��1
2C2H2(g)��5O2(g)��4CO2(g)��2H2O(l) ��H3����2599kJ��mol��1
���ݸ�˹���ɣ�����298Kʱ��C(s)��H2(g)����1molC2H2(g)��Ӧ�ķ�Ӧ��
��H ��______________________��
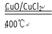 2Cl2��2H2O
2Cl2��2H2O