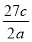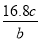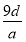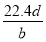题目内容
现有铁和另一种金属组成的混合物,在5.6 g该混合物中加入100 g一定溶质质量分数的稀盐酸,两者恰好完全反应,产生氢气的质量为m。下列说法正确的是( )
A.若混合物为Fe、Al,m可能是0.2 g
B.若混合物为Fe、Zn,m可能是0.2 g
C.若混合物为Fe、Zn,m可能是0.1 g,则该混合物中铁的质量分数为50%
D.若混合物为Fe、Al,则稀盐酸中溶质质量分数一定大于7.3%
D
【解析】A项,若混合物是Fe、Al,m应大于0.2 g,错误;B项,若混合物是Fe、Zn,m应小于0.2 g,错误;C项,若5.6 g全是Fe,则放出H2为0.2 g,若5.6 g全是Zn,则放出H2为 ×2 g>0.1 g,错误;D项,若5.6 g全是Fe,则n(H2)=0.1 mol,m(HCl)=
×2 g>0.1 g,错误;D项,若5.6 g全是Fe,则n(H2)=0.1 mol,m(HCl)=
7.3 g,盐酸的质量分数为7.3%,若5.6 g全是Al,则m(HCl)= ×3×36.5 g≈22.7 g,其质量分数为22.7%,D正确。
×3×36.5 g≈22.7 g,其质量分数为22.7%,D正确。

已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
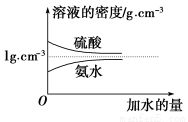
| 溶质的物质的量浓度/mol·L-1 | 溶液的密度/g·cm-3 |
硫酸 | c1 | ρ1 |
氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为________(不写单位,用含c1、ρ1的代数式表示)。
(2)物质的量浓度为c1 mol·L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为________mol·L-1。
(3)物质的量浓度为c2 mol·L-1的氨水与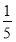 c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________
c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________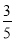 c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
c2 mol·L-1(设混合后溶液的体积变化忽略不计)。