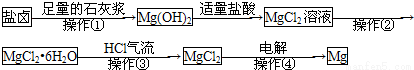
题目内容
某混合物的水溶液中可能含有以下离子:Na+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、SO42-,现取100mL的两份溶液进行如下实验。(己知NH4++OH-=NH3↑+H2O)
① 一份加过量NaOH溶液后加热,收集到0.03mol气体,无沉淀生成,同时得到溶液甲。
② 向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02g固体。
③ 另一份加足量BaCl2溶液后,生成白色沉淀,过滤后的沉淀经量盐酸酸洗涤、干燥后,得到23.3g固体,向滤液中加入AgNO3溶液又有白色沉淀产生。
下列有关叙述正确的是( )
A.由①可知原溶滚存在离子为NH4+,其浓度为0.03mol/L
B.n(NH4+):n(Al3+):n(SO42-)=3:l:10
C.原溶液一定存在Cl-
D.原溶液肯定没有Fe3+、Mg2+,一定含有Na+
练习册系列答案
相关题目

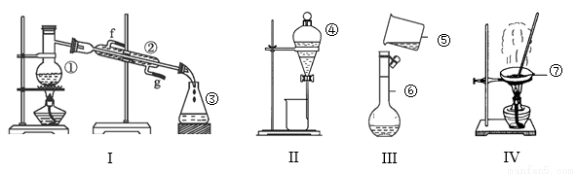
(1)写出下列仪器的名称:③ ,④ ,⑦ 。
(2)以上装置中,不能进行物质的分离与提纯实验的是 (填写相应序号,下同);实验装置不完整的是 ;加热时需加垫石棉网的是 ;实验之前需检查装置气密性的是 。
(3)实验室准备用18 mol/L浓硫酸配制100 mL 3 mol/L稀硫酸。则所需浓硫酸的体积是________ mL(保留一位小数),量取浓硫酸所用量筒的规格是________(选填“10mL”、“25mL”或“50mL”)。在实验操作的摇匀过程中,不慎洒出几滴,此时应采取的措施是 。解决了上述问题后,仍发现所配制的稀硫酸浓度偏大,则下列可能的原因分析中正确的是 。
A.配制前,容量瓶中有少量蒸馏水 |
B.量取浓硫酸时,仰视液体的凹液面 |
C.未经冷却,立即转移至容量瓶定容 |
D.定容时,俯视溶液的凹液面 |


 H2O)制备还原铁粉的步骤如下:将绿矾溶于稀硫酸溶液,向其中滴加(NH4)2CO3溶液,得到FeCO3•nH2O沉淀,静置,过滤,洗涤,干燥,再将FeCO3与煤粉一起焙烧,最终制得还原铁粉。涉及的主要
H2O)制备还原铁粉的步骤如下:将绿矾溶于稀硫酸溶液,向其中滴加(NH4)2CO3溶液,得到FeCO3•nH2O沉淀,静置,过滤,洗涤,干燥,再将FeCO3与煤粉一起焙烧,最终制得还原铁粉。涉及的主要 FeO+CO2,
FeO+CO2,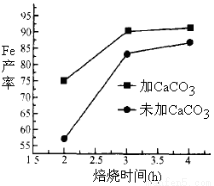
 CO(g)+H2O(g)。
CO(g)+H2O(g)。 反应的化学平
反应的化学平 衡常数表达式K=________。
衡常数表达式K=________。