题目内容
下列分子中所有原子都满足最外层为8电子结构的是
| A.CCl4 | B.H2O | C.BF3 | D.PCl5 |
A
解析试题分析:A、CCl4中碳原子与氯原子形成4对共用电子对,所以所有原子都满足最外层为8电子结构,正确;B、H2O中氢原子满足2电子的稳定结构,错误;C、BF3 分子中B最外层6个电子,不满足最外层为8电子结构,错误;D、PCl5分子中P超过8电子,错误,答案选A。
考点:考查电子式中最外层电子数的判断

练习册系列答案
相关题目
下列过程中,共价键被破坏的是( )
①碘升华 ②溴蒸气被木炭吸附 ③酒精溶于水 ④HCl气体溶于水⑤冰融化 ⑥NH4Cl“升华”⑦氢氧化钠熔化 ⑧(NH4)2SO4溶于水
| A.①④⑥⑦ | B.④⑥⑧ | C.①②④⑤ | D.④⑥ |
下列用电子式表示的形成过程正确的是( )
A. |
B.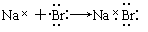 |
C. |
D. |
下列关于离子化合物的叙述正确的是:
| A.离子化合物中都含有离子键 |
| B.离子化合物中的阳离子只能是金属离子 |
| C.离子化合物如能溶于水,其水溶液一定可以导电 |
| D.溶于水可以导电的化合物一定是离子化合物 |
关于离子键、共价键的各种叙述中正确的是( )
| A.在离子化合物里,只存在离子键,没有共价键 |
| B.非极性键只存在于双原子的单质分子(如Cl2)中 |
| C.由不同元素组成的多原子分子里,一定只存在极性键 |
| D.共价化合物分子中,一定不存在离子键 |
根据化学反应的实质是旧键的断裂和新键的形成这一现实,下列变化不属于化学反应的是( )
| A.白磷在260 ℃时转化为红磷 | B.石墨在高温下转化为金刚石 |
| C.NaCl熔化 | D.五氧化二磷吸水 |
下列共价化合物的电子式正确的是( )。
A. (NH3) (NH3) | B. ∶∶ ∶∶ H(H2O2) H(H2O2) |
C.∶ ∶(CO2) ∶(CO2) | D. (HClO) (HClO) |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为( )
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 |
| D.以上说法都不正确 |
下列变化是在克服分子间作用力的情况下进行的是( )。
| A.碘的升华 | B.氨的液化 |
| C.铝的熔化 | D.食盐的溶解 |