题目内容
在CuSO4和FeSO4的混合溶液中加入Mg粉,下列说法错误的是
- A.若Mg粉有剩余,溶液中只有Fe2+,而无Mg2+和Cu2+
- B.若Mg粉无剩余,溶液中如有Cu2+,则必定有Fe2+
- C.若Mg粉有剩余,溶液中只有Mg2+,而无Fe2+和Cu2+
- D.若Mg粉无剩余,溶液中无Cu2+,则一定有Mg2+和Fe2+
A
分析:A、依据金属活动顺序表中的金属活泼性分析,镁和在CuSO4和FeSO4的混合溶液能发生置换反应;
B、依据金属活动顺序表中的金属活泼性分析,氧化性Cu2+>Fe2+,氧化还原反应顺序进行;
C、依据金属活动顺序表中的金属活泼性分析,镁和在CuSO4和FeSO4的混合溶液能发生置换反应;
D、依据金属活动顺序表中的金属活泼性分析,氧化性Cu2+>Fe2+,氧化还原反应顺序进行.
解答:A、镁和在CuSO4和FeSO4的混合溶液能发生置换反应;氧化性Cu2+>Fe2+,溶液中一定含有Mg2+,故A错误;
B、依据金属活动顺序表中的金属活泼性分析,氧化性Cu2+>Fe2+,氧化还原反应顺序进行,若Mg粉无剩余,溶液中如有Cu2+,镁分全部和铜离子反应,所以则必定有Fe2+,故B正确;
C、依据金属活动顺序表中的金属活泼性分析,氧化性Cu2+>Fe2+,氧化还原反应顺序进行,若Mg粉有剩余,Fe2+和Cu2+全部反应,溶液中只有Mg2+,故C正确;
D、依据金属活动顺序表中的金属活泼性分析,氧化性Cu2+>Fe2+,氧化还原反应顺序进行,若Mg粉无剩余,铜离子全部反应,亚铁离子部分反应,溶液中无Cu2+,则一定有Mg2+和Fe2+,故D正确;
故选A.
点评:本题考查了金属活动顺序表的应用,主要是金属间的置换反应应用,阳离子的氧化性顺序是判断的依据.
分析:A、依据金属活动顺序表中的金属活泼性分析,镁和在CuSO4和FeSO4的混合溶液能发生置换反应;
B、依据金属活动顺序表中的金属活泼性分析,氧化性Cu2+>Fe2+,氧化还原反应顺序进行;
C、依据金属活动顺序表中的金属活泼性分析,镁和在CuSO4和FeSO4的混合溶液能发生置换反应;
D、依据金属活动顺序表中的金属活泼性分析,氧化性Cu2+>Fe2+,氧化还原反应顺序进行.
解答:A、镁和在CuSO4和FeSO4的混合溶液能发生置换反应;氧化性Cu2+>Fe2+,溶液中一定含有Mg2+,故A错误;
B、依据金属活动顺序表中的金属活泼性分析,氧化性Cu2+>Fe2+,氧化还原反应顺序进行,若Mg粉无剩余,溶液中如有Cu2+,镁分全部和铜离子反应,所以则必定有Fe2+,故B正确;
C、依据金属活动顺序表中的金属活泼性分析,氧化性Cu2+>Fe2+,氧化还原反应顺序进行,若Mg粉有剩余,Fe2+和Cu2+全部反应,溶液中只有Mg2+,故C正确;
D、依据金属活动顺序表中的金属活泼性分析,氧化性Cu2+>Fe2+,氧化还原反应顺序进行,若Mg粉无剩余,铜离子全部反应,亚铁离子部分反应,溶液中无Cu2+,则一定有Mg2+和Fe2+,故D正确;
故选A.
点评:本题考查了金属活动顺序表的应用,主要是金属间的置换反应应用,阳离子的氧化性顺序是判断的依据.

练习册系列答案
相关题目
下列有关含铜化合物的说法错误的是(设NA为阿伏加德罗常数的值)( )
| A、用盐酸可以洗去铜表面的铜锈 | B、0.1mol?L-1的CuSO4溶液中,Cu2+的数目一定小于0.1NA | C、在CuCl2和FeCl3的混合溶液中加入铁粉,若有固体残留,则其中一定含有铜 | D、在FeSO4溶液中加入CuS固体,溶液中c(Fe2+)不变,说明K甲(CuS)远小于K甲(FeS) |
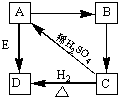 Ⅰ.下列各组物质是按一定规律排列的,请将对应的排列依据填在括号内.
Ⅰ.下列各组物质是按一定规律排列的,请将对应的排列依据填在括号内.